
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

���ľ�ѡ
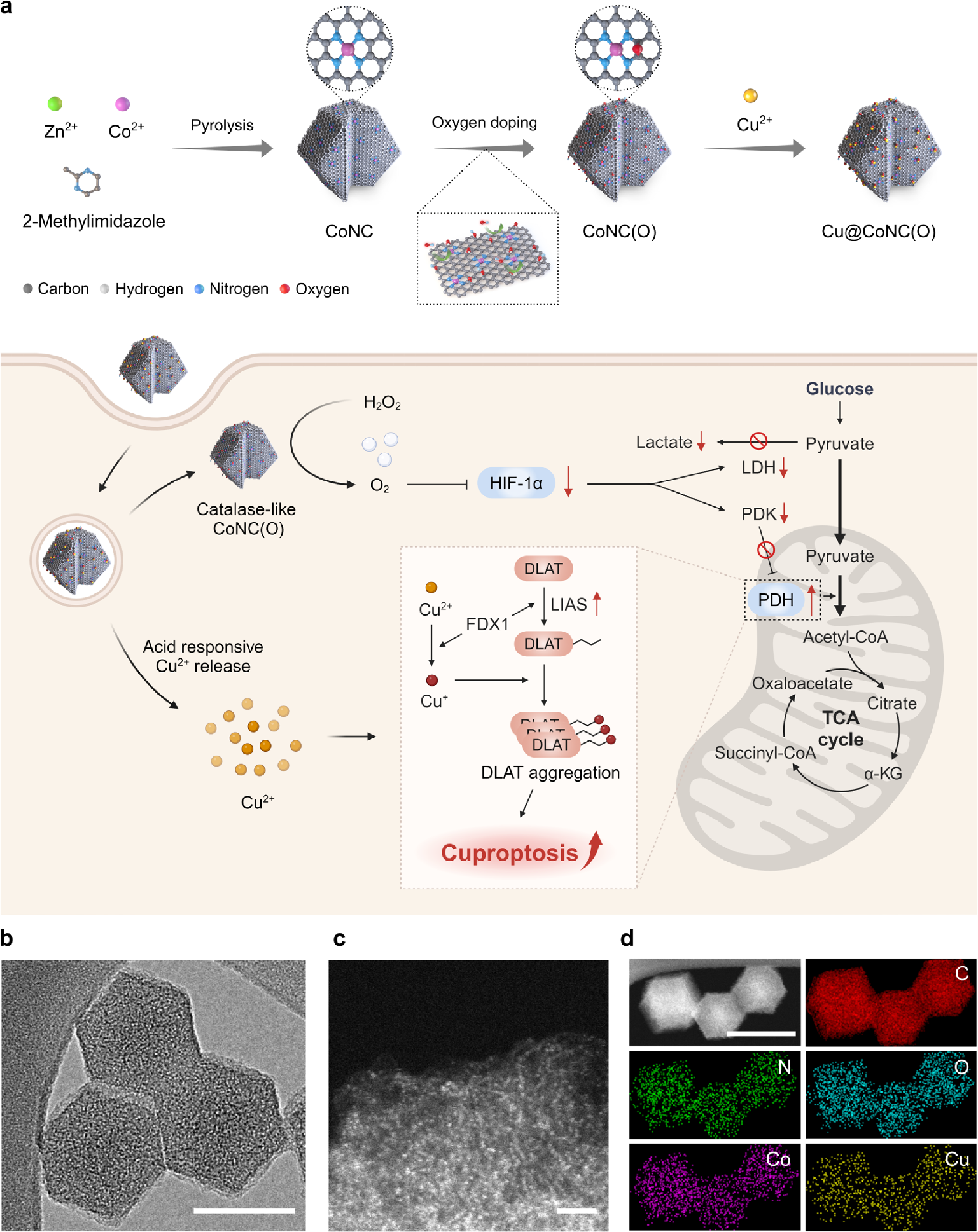
ͭ������ϸ��������һ��ͭ������ϸ������������ʾ����Ϊһ���������嵰�ۼ�Ϊ�����İ�֢�Ʒ���ǰ����Ȼ������һ���ص�����ʹ����Ч�߶������ڰ�ϸ���Ĵ�л״̬������������Խ��͵�ȱ�������в�������Ԥ���ڴˣ�����ʹ�ø����ܵ�ԭ������ø ��Cu@CoNC��O���� ������һ�־��й�������ø�����Ե� Cu �������壬���ڵ���ͭ��ͬʱ�ر�̴�л��ͨ������������������̼�����ϣ�Cu@CoNC��O�� ��ȱ����Ӧ����ȣ�Cu ���ӵĸ���Ч��������ߡ�ͬʱ��Cu@CoNC��O�� ��ɫ�Ĺ�������ø�����Կɻ���ȱ����ͨ�����������л�ͼ�����ͪ������ø������������л���ǽͽ�ת��Ϊ�������������ʹ��ȱ�������£���лת�ƺ���Ч Cu ���͵�Эͬ����Ҳ�ܴٽ� Cuproposis���Ӷ���ǿ����Ч�������о�֤���˵�ԭ������ø��Ϊ�����ӵ��������DZ�����ܹ�ͬʱִ�д����ܺ͵��ͽ������ӣ������һ��ͨ����л������ǿ cupropsosis ����Ч���ԡ�
����ҽѧӦ��
������øƽ̨ͨ����л�ر�̲��ԣ����Ȱ����������쳣/�ǽͽ������������������ٰ����ΰ������ٰ��������ϷŻ���/����������ǿ��Ч���������һ�廯���ܣ���ͭ����ԭ������ø��PET������ʵʱ�������ֲ����л�仯��ʵ�־���Ԥ����չӦ�����������Լ���������������л/������̬����ȱѪ�ٹ�ע���ˣ�����ȱ��/��л���ң�����ά��/��Ⱦ�Լ��������ش�л�ر�̣��ȴ�л��ؼ������ơ�
ԭ������
ACS Nano ( IF 16 )
Pub Date : 2025-06-11
DOI: 10.1021/acsnano.5c00012
Kang Kim, Jaewoo Lee, Ok Kyu Park, Hyochul Lee, Taekyu Jang, Jungho Kim, Bowon Lee, Jeong Hyun Kim, Jaeho Moon, Seoin Back, Nohyun Lee, Seung Hong Choi, Taeghwan Hyeo
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ