
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

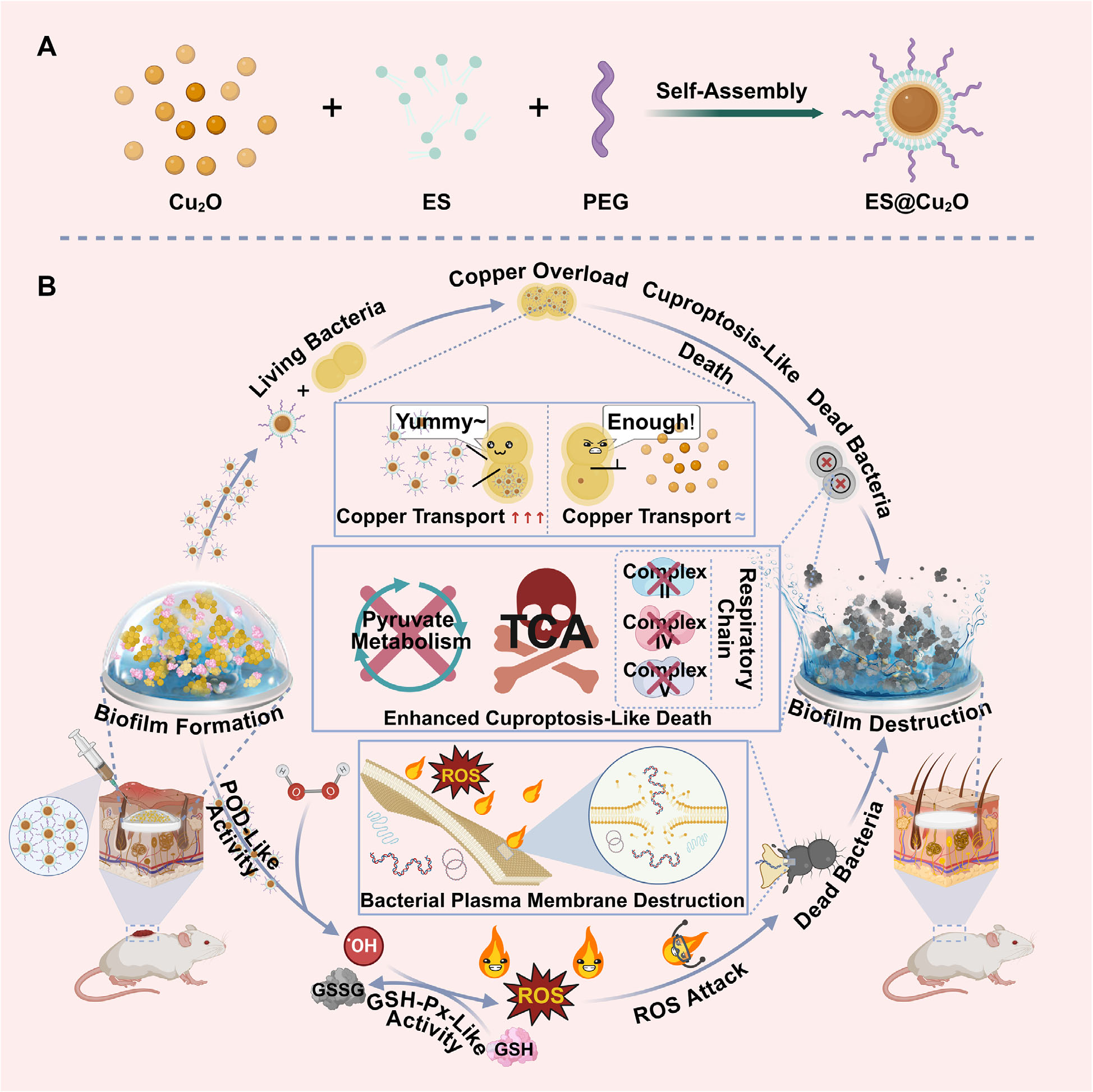
��ϸ������Ĥ��ֳ�鵼��ֲ������ظ�Ⱦ���ǵ��¹ǿƼ���ʧ�ܵ���Ҫԭ����Ȼ��ͳ���������ط����ٴ���Ч���ޣ������崴��������壬�������Ԥ�����ߴ����˾�������;��ø�����ΪӦ����һ��ս��ͨ����ͭ��������������Cu 2 O NPs����ͭ������ elesclomol��ES�����ϣ����̻��˾���˫ø���Ե� ES@Cu 2 O ����ø��ּ��ͨ����ǿͭ�ܶ������������Կ�ֲ����ظ�Ⱦ��ES@Cu 2 O ����ø���ù�������ø����POD-like�����Դ���Դ�Թ������⣨H 2 O 2��ת��Ϊ��������ROS����������Ĥ�����в���ǿ����������ӿ��ͬʱ��ES@Cu 2 O �Ĺ����Ĺ�������ø����GSH�\Px ����������Ч���Ĺ�����Ĺ����ģ�GSH�����Ӷ����� ROS �鵼������Ч����ֵ��ע����ǣ�ES ��Ӿ��쳣��ϸ���� Cu 2+���ۣ��Ӿ�������ϩ������֢���������� Cu-2O ��������ȣ�ES@Cu 2O ������������չ�ֳ�������ǿ�Ŀ���������Ĥ����������RNA ����RNA-seq����ʾ���� ES@Cu 2 O �������У��ؼ���������л;�������� TCA ѭ������ͪ���л���������ữ������� Cu-2 O �������������ƣ�֧�� ES �鵼�� Cu 2+����ǿ����ǿͭ-���ữ�������Ļ��ơ� �����ڣ�ES@Cu 2 O ��С��ֲ����ظ�Ⱦģ���б��ֳ�����Ŀ�������Ч���������ﰲȫ����֤ʵ��ȫ�����Կɺ��Բ��ơ�������ԣ����о���ʾ������˫ø���Ե� ES@Cu 2 O ����øͨ����ǿ���Ʒ䳲�����������ܹ�ǿ������������Ĥ������ֲ����ظ�Ⱦ�еĶ�ֲϸ���������һ�־��������ٴ�ת��DZ���������Ʋ��ԡ�

�ڹǿ������У��˹�ֲ�����ѳ�Ϊ���������ȶ����ܵĹؼ����ߡ�Ȼ������Щֲ����ı��漫�׳�Ϊϸ��𤸽�Ͷ�ֲ���´���һ���γɽṹ���ܡ�����������ʵ����ﱻĤ�����������̵�ֲ������ظ�Ⱦ�����ﱻĤ��ͬϸ���ġ����ݡ��������ܵ�����������ϵͳ�Ĺ�������ʹ��Կ����ز�����ǿ����ҩ�ԣ����´�ͳ�������������Ʒ���������Ч���������������ò����ܶ����崴�����û�ֲ����ľ����ĺ;��ø�������ˣ�����һ���ܹ���Чͻ�����ﱻĤ���ϡ����������ԭ���ķ������Ʒ�����Ϊ�ٴ�ؽ����������⡣
�����һ��ս��һ�������о������һ�ִ��µ�����ø���ԡ��о���Ա�ɹ�������һ�ָ���ͭ�������尬����Ī��Elesclomol�� ES����������ͭ����ø��ES@Cu2O���������������ײ��Ͼ���˫��ø���ԣ������ﱻĤ���е����������У����ܹ����������øһ��������Դ�Թ������������������ǿɱ�����Ļ����������ⲿ�������ﱻĤ��ͬʱ��������ģ������Ĺ�������ø�Ĺ��ܣ���Ч�������ﱻĤ�й��ȱ���Ļ�ԭ�����ģ��Ӷ�����ϸ���Ŀ����������������Ŵ���������ƻ�ЧӦ��
��Ϊ������ǣ����صİ�����Ī�����ˡ�������ľ������Ĺؼ����á����ܹ�Ю��ϸ����Ĥת��ϵͳ���ƹ���������ͭ���ӵ�����أ�ͬʱ�������űõĹ��ܣ��Ӷ���������ͭ���ӡ�͵�ˡ���ϸ��ϸ�����ڲ������ֲ���ֱ���ƻ���ϸ���ڲ���ͭ������̬������ͭ�����쳣�����������ͭ���ӻ���������ѭ���е�������������ϣ������ؼ����Ѿۻ����ƻ�����ص�����ͬʱ���ظ��������������ĵ��Ӵ��ݣ������յ�ϸ������һ�����ơ�ͭ������������������ʽ��
����ʵ��֤ʵ���뵥����������ͭ��������ȣ�ES@Cu2O����ø���ͼ������ֽ��ɫ��������ʹ˾���չ�ֳ�������ǿ��ɱ����������ﱻĤ������ͨ��RNA����������������֣���ES@Cu2O������ϸ������������ѭ������ͪ���л���������ữ�Ⱥ���������лͨ·�еĹؼ�������ﱻ�㷺�����������ƣ���ӷ��Ӳ���ֱ����֤��ES�鵼��ϸ����ͭ���ӳ����ܹ���Ч�Ӿ�ϸ���ġ�ͭ���������������̡�
�ڶ���ģ��ʵ���У�ES@Cu2Oͬ�����ֳ�Խ������Ч������С��ֲ�����Ⱦģ���У���ES@Cu2O���ϵ�Ũ�ȹ����������Ƶ�������Ⱦ��λδ�������Եĺ�ߡ�ˮ�����ã�ֲ�����������ﱻĤ����Χ��֯�еIJ���ϸ��������������٣���֯ѧ��Ƭ��ʾ��֢ϸ�������������ᣬ���������õ���֯������ϵͳ�����ﰲȫ������Ҳ�������ò�������Ч����Ũ������Ѫ�ʵͣ�����Ҫ�����������ˣ�չ�ֳ����õ����������ԡ�
�����о�������ø��˫�ش�������ͭ��������İ�����������ϣ�������һ��������Ӧ���ﱻĤ������Эͬ����ϵͳ��������ͨ�������������������Ŀ����������ⲿ�߽����ﱻĤ����ͨ���յ�ϸ���ڲ��ġ�ͭ�������������Ӹ�Դ��ɱ��ϸ����Ϊ������ҩ��ֲ������ظ�Ⱦ�ṩ��һ�ּ���DZ�����²��ԡ�δ�������Ź�ģ���Ʊ����յ��Ż��ͳ��ڰ�ȫ�����۵���ɣ���һ��������ƽ̨����Ϊ�ٴ�����ǿ�ֲ�����Ⱦ��һ������������µ���⡣
�ο���Ϣ��
DOI: 10.1002/adfm.202524044
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ