
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

结直肠癌(CRC)的免疫治疗在临床上仍受限于极度免疫抑制的肿瘤微环境。核系杆菌(Fn)选择性定殖于 CRC 肿瘤,通过在巨噬细胞内持续存在并驱动其 M2 极化,驱动免疫抑制。我们设计了一种自激活的高分子纳米酶,该酶由含铁辛糖聚合物和青蒿酸(AS)载荷组成,用于消除巨噬细胞内 Fn 储存库并重编程巨噬细胞免疫生态系统。这些纳米酶通过甘露糖受体介导的胞吞作用被 M2 样 Fn 感染的巨噬细胞特异性吞噬,随后被细胞内过表达的过表达氢激活,释放亚铁离子和 AS,通过芬顿化学协同扩增细胞毒性活性氧(ROS)生成。同时,AS 诱导巨噬细胞自噬,促进纳米酶-细菌在自噬酶体中的共定位,以增强 ROS 介导的 Fn 杀伤。值得注意的是,细胞内 Fn 的根除不仅逆转了感染巨噬细胞的免疫抑制表型,还触发了旁分泌信号,驱动邻近未感染巨噬细胞的 M1 再极化。在含有细胞内 Fn 的异种移植和正位 CRC 模型中,纳米酶能够高效消除细胞内 Fn,并系统性重塑巨噬细胞免疫结构,显著提升抗 CD47 免疫疗法的治疗效果。本研究提出了一种通过精准靶向肿瘤相关巨噬细胞内细菌来改进 CRC 免疫治疗的策略。

该研究以题为“Engineered Self-Activatable Polymeric Nanozymes Precisely Eradicate Tumor-Associated Intramacrophage Bacteria to Potentiate Immunotherapy Based on Cluster of Differentiation 47 Blockade”发表在ACS Nano上。
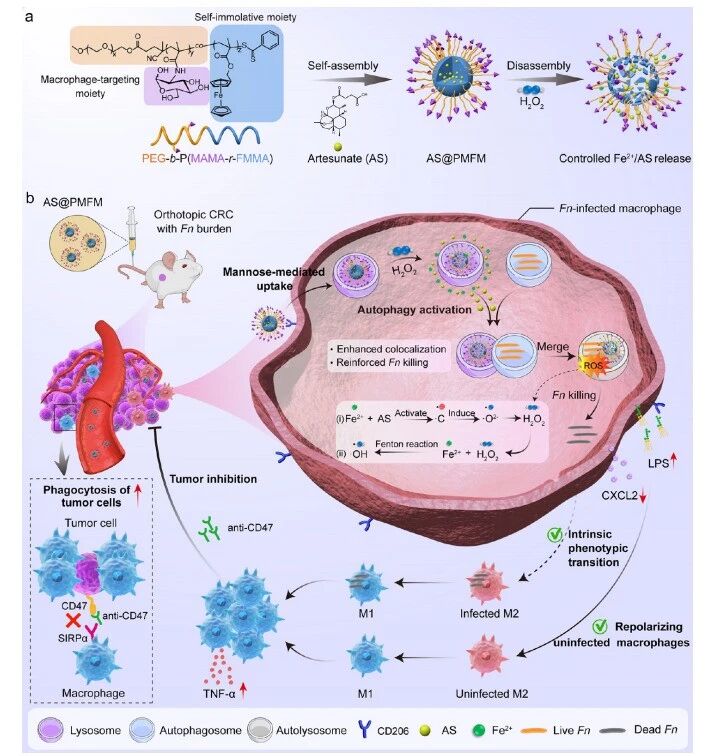
(a)巨噬细胞靶向自激活聚合物纳米酶平台(AS@ PMFM )的自组装与H2O2诱导解组装示意图;(b)AS@ PMFM 在正位结直肠癌小鼠模型中对Fn负荷的治疗机制
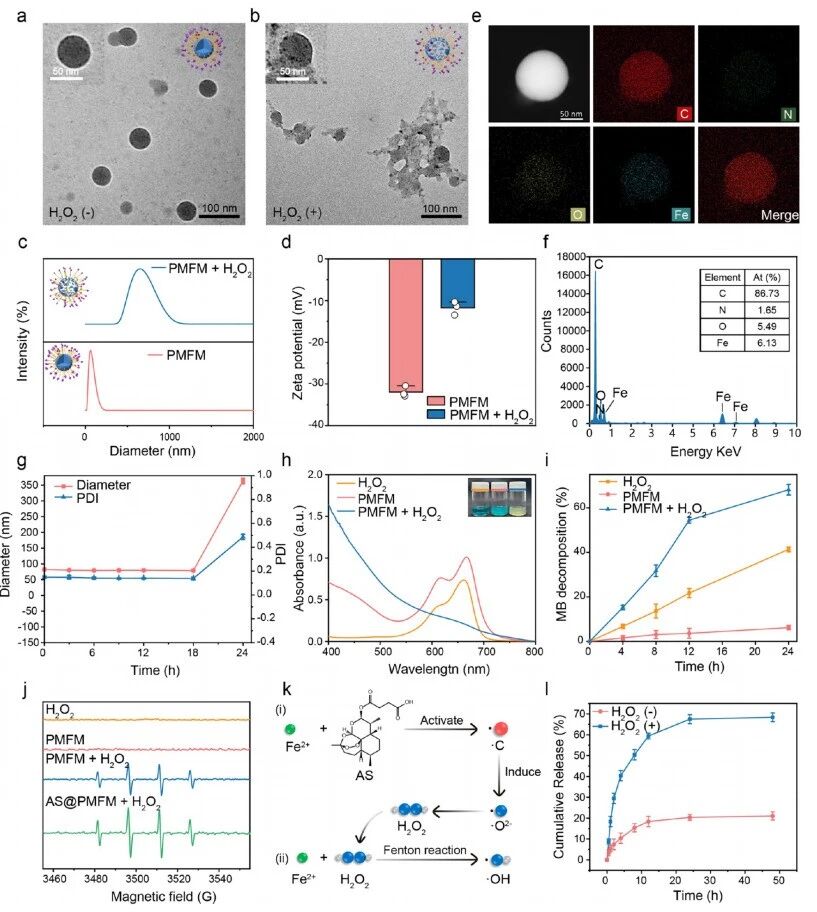
PMFM 胶束的表征。(a,b) PMFM 胶束在过氧化氢(200 mM)作用下的TEM图像(a)和 PMFM 胶束。(c,d) 通过DLS在173°C下测定的 PMFM 胶束在有或无过氧化氢(200 mM)存在时的粒径分布(c)和 ζ 电位(d)。(e,f) PMFM 胶束的 HAADF -STEM图像(e)和EDS元素分析(f)。(g) 纳米颗粒尺寸和PDI在有或无过氧化氢存在时的变化。(h,i) UV−vis光谱(h)和MB在有或无过氧化氢(200 mM)存在时的分解速率(i)。(j) PMFM 和AS@ PMFM 在有或无过氧化氢存在时的ESR光谱。(k) Fe2+与AS协同作用产生ROS的过程。(l) AS@ PMFM 在有或无过氧化氢存在时的体外AS累积释放。
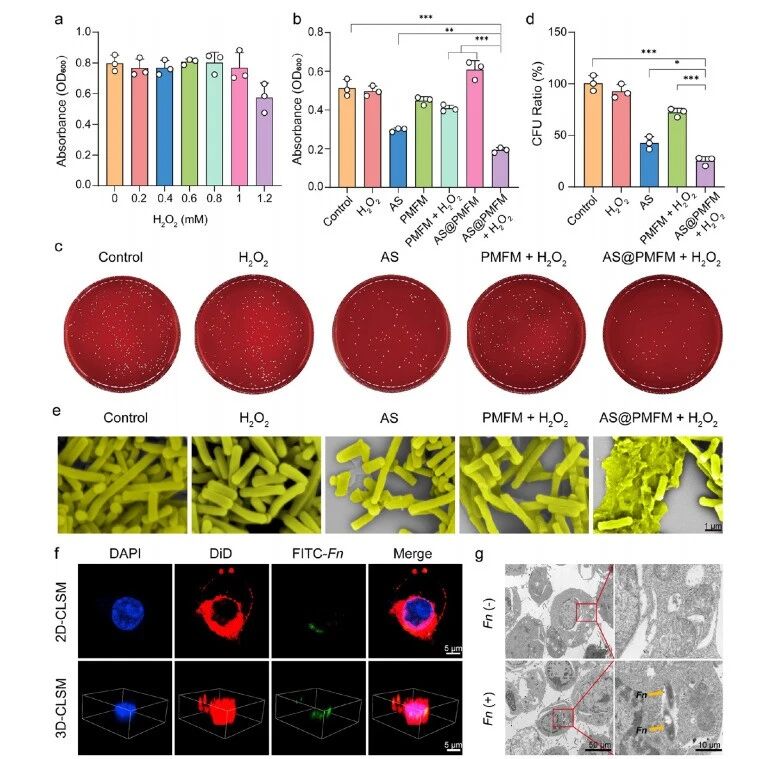
细胞外抗菌效应及Fn在巨噬细胞内驻留的测定。(a) Fn经不同浓度过氧化氢处理24小时后的OD600值。(b) 经不同处理24小时后Fn的OD600值。(c,d) 经不同处理24小时后Fn的菌落平板图像(c)及 CFU 率(d)。(e) 不同处理后Fn的代表性SEM图像。(f) RAW264.7细胞内 FITC 标记Fn的平面(2D)和z-stack(3D) CLSM 图像(MOI = 20)。(g) 未感染与Fn感染的RAW264.7细胞的TEM图像(黄色箭头指示细胞内的Fn),Fn(+)和Fn(−)分别指添加Fn或未添加Fn。数据以均值±标准差表示(n = 3)。***p < 0.001,**p < 0.01,*p < 0.05。
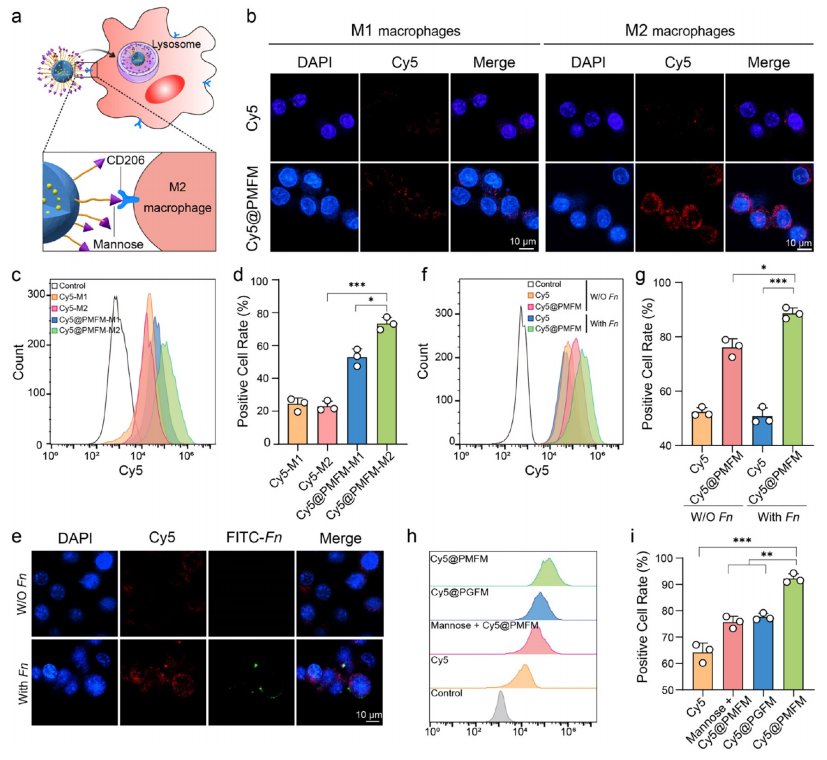
M2型巨噬细胞特异性内化过程。(a) AS@ PMFM 通过甘露糖受体介导的内吞途径进入M2型巨噬细胞。(b−d) CLSM 图像(b)及流式细胞术分析(c,d)显示M1型或M2型巨噬细胞与游离Cy5或Cy5@ PMFM 共孵育3小时后的结果。(e−g) CLSM 图像(e)及流式细胞术分析(f,g)显示未感染或Fn感染巨噬细胞与Cy5@ PMFM 共孵育3小时后的结果。(h,i)流式细胞术分析显示Fn感染巨噬细胞经不同处理3小时后的结果。数据以均值±标准差表示(n=3)。***p<0.001,**p<0.01,*p<0.05。
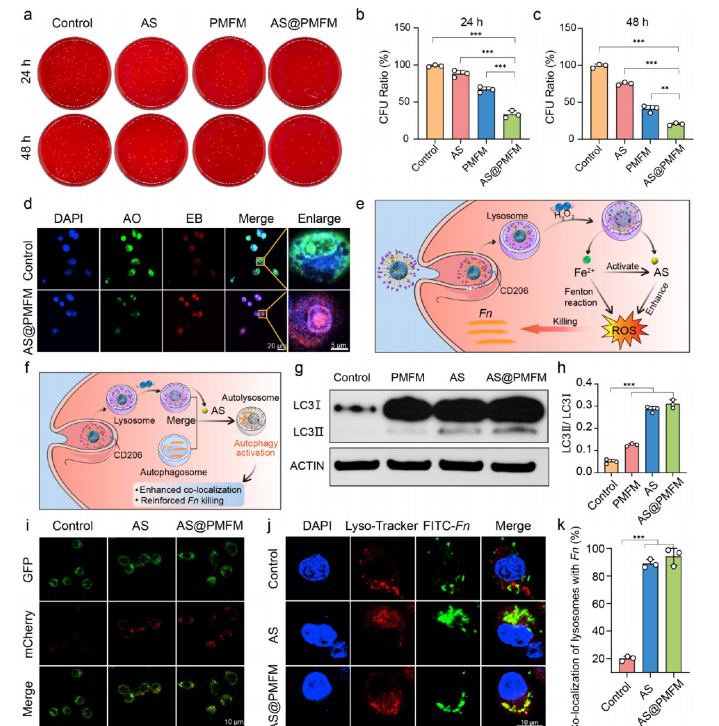
自噬激活驱动的细胞内抗菌活性。(a−c)菌落平板图像(a)及Fn在不同处理24小时(b)和48小时(c)后的 CFU 比。(d)AS@ PMFM 处理后Fn的AO和EB荧光染色。(e)AS@ PMFM 清除细胞内Fn的流程示意图。(f)AS@ PMFM 激活巨噬细胞自噬的机制示意图。(g,h)不同处理后RAW264.7细胞的蛋白质印迹(g)和蛋白定量(h)。(i)不同处理后自噬体-溶酶体融合的 CLSM 图像。(j)不同处理后溶酶体与Fn共定位的 CLSM 图像。(k)溶酶体与Fn共定位的百分比。数据以均值±标准差表示(n=3)。***p<0.001,**p<0.01。
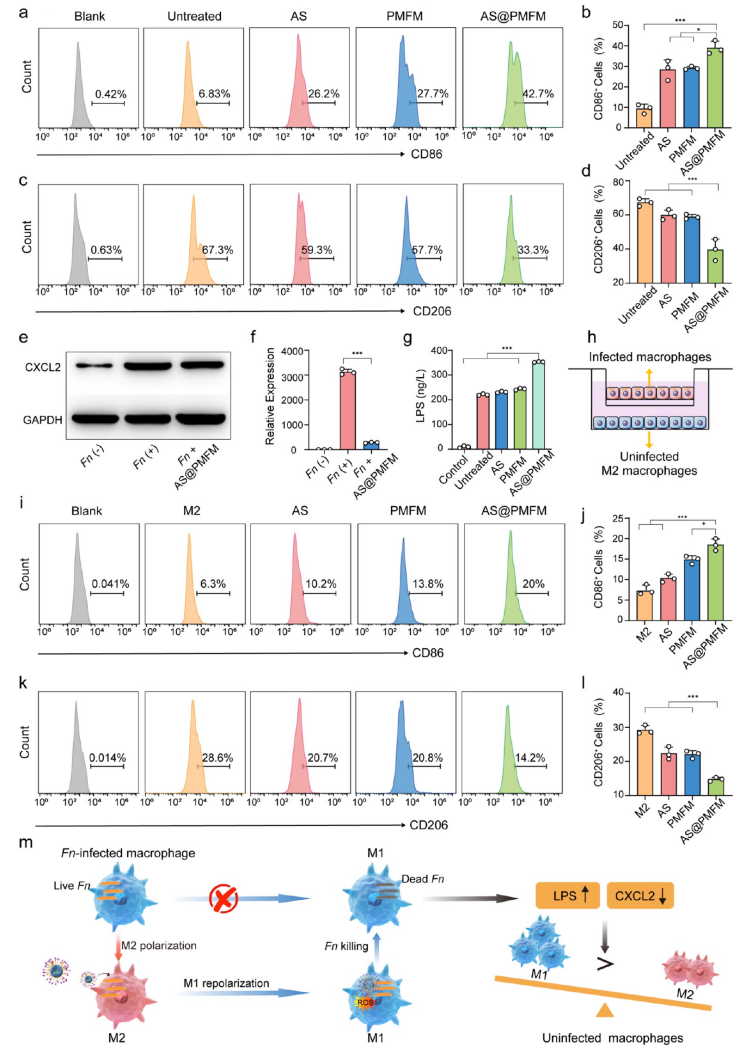
Fn感染与未感染M2巨噬细胞在细胞内Fn杀伤作用下的M1复极化。(a) 不同处理后CD86表达的流式细胞术分析。(b) 流式细胞术对CD86阳性细胞百分比的定量分析。(c) 不同处理后CD206表达的流式细胞术分析。(d) 流式细胞术对CD206阳性细胞百分比的定量分析。
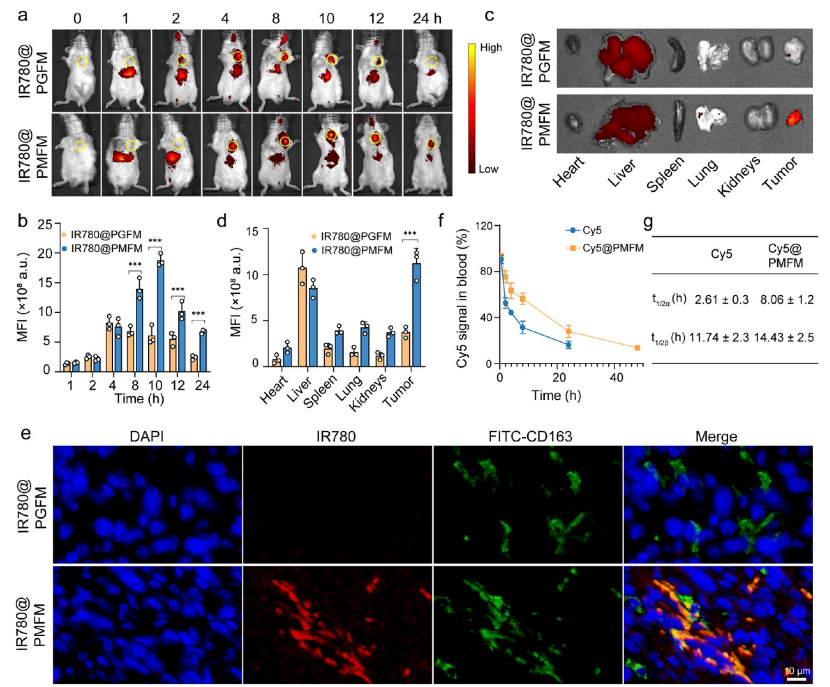
体内生物分布与药代动力学测定。(a,b) 通过尾静脉注射至CT26荷瘤小鼠后不同时间点的IR780@ PGFM 与IR780@ PMFM 胶束生物分布(a)及IR780荧光强度定量(b)。(c,d) 给药24小时后离体器官及肿瘤的成像(c)与IR780荧光定量(d)。(e) IR780@ PGFM 或IR780@ PMFM 胶束与M2巨噬细胞的体内共定位。(f) 游离Cy5与Cy5@ PMFM 胶束的药代动力学。(g) Cy5与Cy5@ PMFM 的药代动力学指标(t1/ 2α :药物在血液中的分布半衰期,t1/ 2β :药物在血液中的消除半衰期)。数据以均值±标准差表示(n=3)。***p<0.001。
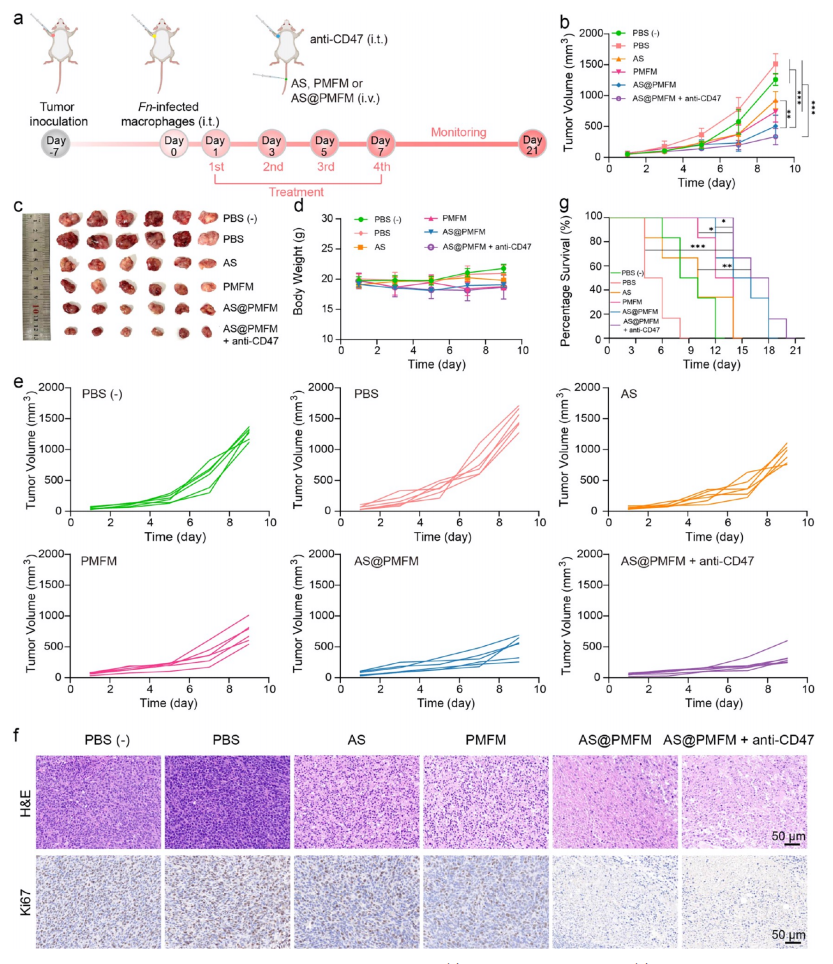
皮下结直肠肿瘤模型的体内抗肿瘤疗效。(a) 体内治疗时间线。(b) 不同治疗组小鼠的肿瘤生长曲线。PBS(−)表示未进行细胞内Fn预感染的PBS处理组。(c) 治疗结束时获取的小鼠肿瘤照片。(d) 不同治疗组荷瘤小鼠体重变化情况。(e) 各治疗组小鼠个体肿瘤生长曲线。(f) 不同治疗组肿瘤组织的H&E染色与Ki67标记图像。(g) 21天周期内各治疗组小鼠的生存率。数据以均值±标准差表示(n=6)。***p<0.001,**p<0.01,*p<0.05。
总结
结直肠癌里有一种叫具核梭杆菌的厌氧菌,它不仅能在肿瘤里存活,还特别擅长躲进巨噬细胞里,把原本应该杀肿瘤的免疫细胞“策反”成M2型促癌表型,让以CD47为代表的免疫检查点疗法在多数患者身上失灵。最近,天津工业大学高辉团队在《ACS Nano》发表了一项研究,他们设计了一种能自己“觉醒”的聚合物纳米酶,专门解决这个难题。这个纳米颗粒表面修饰了甘露糖,能精准识别M2型巨噬细胞上高表达的CD206受体,钻进细胞后,遇到细菌感染带来的高浓度过氧化氢,颗粒里的二茂铁模块迅速释放亚铁离子,同时把装载的青蒿琥酯也放出来。亚铁离子和青蒿琥酯联手,通过芬顿反应和过氧桥键断裂,在局部掀起一场活性氧风暴,把藏在自噬溶酶体里的具核梭杆菌清理干净。
体外数据显示,这种纳米酶能在48小时内清除掉80%以上的胞内细菌,组合指数0.73,说明两种成分有明确的协同效应。更重要的是,把细菌干掉之后,那些被“带偏”的巨噬细胞开始往回走――M1型标志物CD86从20%涨到30%,M2型标志物CD206从81%降到53%。这还没完,清除了细菌的巨噬细胞还会释放脂多糖,同时减少CXCL2的分泌,相当于给周围的巨噬细胞发信号,把它们也往M1方向推。在皮下瘤和原位瘤两个小鼠模型里,这种纳米酶联合CD47抗体,把肿瘤生长摁得死死的,M1/M2比例从0.43拉到2.46,血清TNF-α涨了1.7倍,IL-10降了45%,中位生存期延长到50天。这套“清内鬼、拉帮结派”的策略,算是给难治性结直肠癌的免疫治疗找到了一个新支点。
参考消息:
DOI: 10.1021/acsnano.5c15423
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫