
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

复杂脑部疾病的治疗方法开发面临重大挑战,原因是生物结构复杂且血脑屏障严格。尽管纳米医学充满希望,但传统的研发模式存在低效问题。本综述引入了一种智能治疗型理论范式,整合了高精度脑类器官模型、高通量筛查(HTS/HCS)和人工智能(AI)。在这一闭环工作流程中,类器官平台承担诊断角色,生成纳米医学性能的预测数据。随后,AI 通过处理这些数据,提供治疗指导,推动理性药物设计、合成和相互作用预测。这场人工智能驱动的融合有望显著加速精准定位和个性化纳米医学的发展,为治疗脑部疾病带来新的希望。

该研究以题为“AI and organoid platforms for brain-targeted theranostics.”发表在Theranostics上。
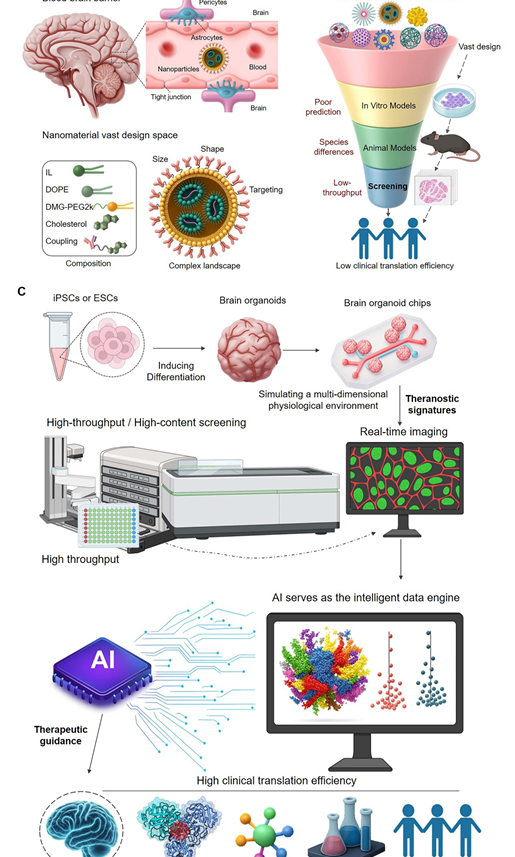
从线性工作流程到整合的诊疗范式。(A) 脑部递送中的诊疗挑战。血脑屏障(BBB)构成了极大的障碍。进一步加剧这一挑战的是纳米颗粒(NPs)的庞大设计空间,使得预测哪些候选者不仅能够穿越BBB,还能实现预期的治疗效果,变得异常困难。(B) 脱节的传统研发工作流程。传统的线性流程效率低下,因为它将测试与设计分开。其依赖预测性差的体外和动物模型构成了不可靠的“诊断”步骤,导致高失败率和潜在“治疗药物”的临床转化率低。(C) 整合的诊疗范式。这种新方法闭合了诊疗循环。高保真模型如脑类器官和类器官芯片作为“诊断平台”,通过高通量筛选生成可预测的数据。人工智能(AI)作为核心引擎,处理这些诊断数据以提供“治疗指导”――理性地设计和优化纳米药物。这种诊断与治疗的整合有望显著提高开发有效脑靶向纳米药物的成功率。
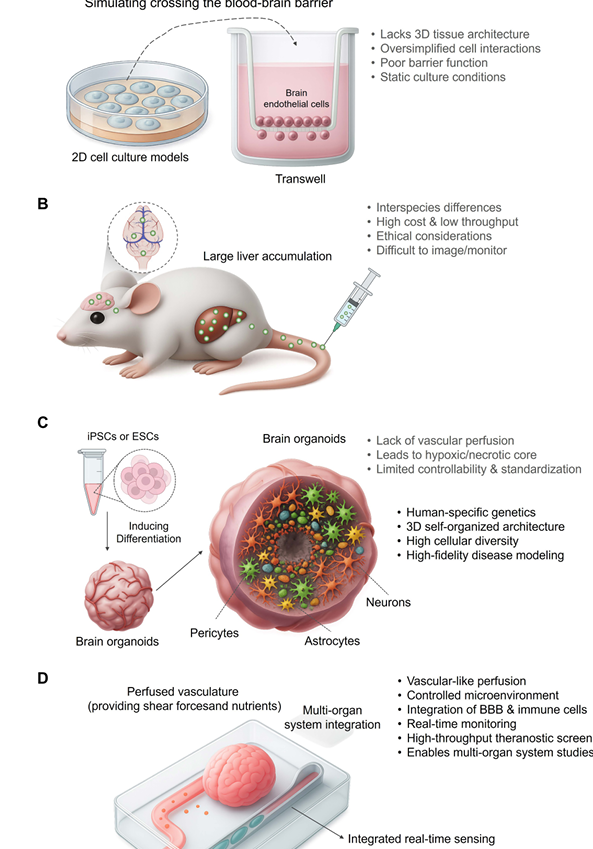
临床前模型向高精度治疗性平台的演变。(A)传统的体外模型提供低保真度的诊断数据。简单的二维培养和Transwell系统虽然是基础,但缺乏三维结构、细胞相互作用过于简化以及屏障功能较差。这些限制严重降低了其体内表现的预测能力,导致候选人选择时诊断信息不可靠。(B)动物模型提供了系统性背景,但可迁移性较差。体内模型面临重大挑战,包括物种间差异、高成本和伦理考量。关键是,它们常常无法预测人类特异性的反应(例如纳米颗粒在肝脏而非大脑中积累),使其成为开发针对人类治疗的平台,翻译不佳。(C)脑类器官代表了向人类相关治疗型建模迈出的一步。这些类器官源自人类iPSC或ESC,重现了人类大脑发育的关键特征,包括人类特异性遗传学和复杂的细胞多样性。这使得高精度的疾病建模成为可能,为评估纳米药物提供了更相关的背景。然而,缺乏血管灌注和标准化有限等限制,仍限制了其作为强健治疗型平台的全部潜力。(D) 脑类器官芯片(BOoC)系统作为集成的治疗型平台出现。通过将类器官集成到微流控器件中,BOoC技术克服了静态培养的诸多局限。它提供了一个受控、渗透的微环境,支持工程化BBB的集成,并支持实时监控。这些特性使BOoC系统成为高通量、生理相关脑靶向另一种病假筛查的最先进临床前平台。
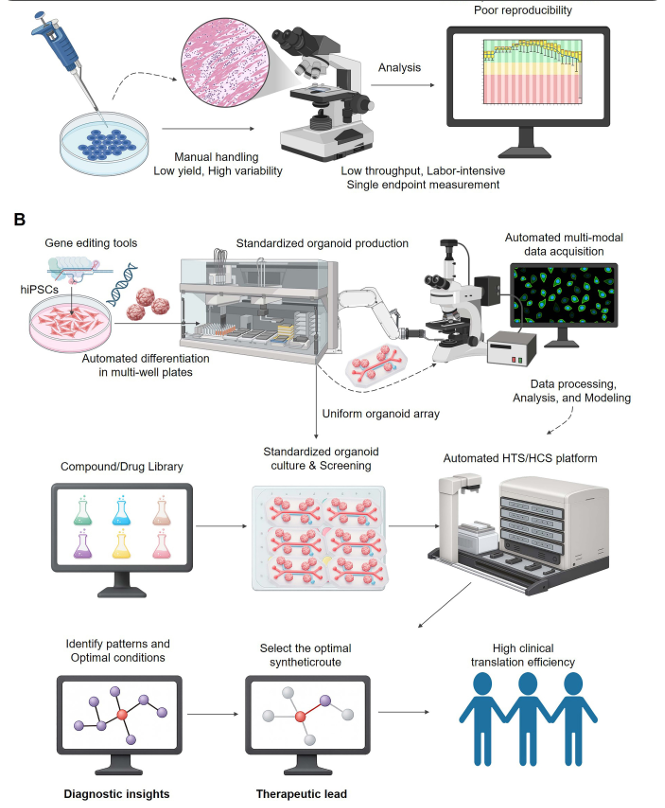
从手动筛选到自动化治疗诊断平台。(A) 传统的手动筛选工作流程对于治疗诊断研发来说是不够的。该过程以手工操作为特征,导致产率低、变异大且可重复性差。依赖劳动密集型、低通量的分析仅能提供有限、低维度的数据,使得系统性评估开发有效治疗诊断所需的复杂相互作用几乎不可能。(B) 自动化 HTS/HCS 平台推动现代治疗诊断工作流程。这一整合模式从标准化、自动化生产均一器官类器官阵列开始,通常来自基因编辑的人诱导多能干细胞(hiPSCs)。随后,自动化 HTS/HCS 平台对这些培养物进行大规模化合物库的筛选。自动化、多模式数据采集生成大规模、高维度的数据集,作为分析和建模的“诊断”输入。这使得能够识别生物学模式并选择最佳候选物,直接将诊断筛选与治疗开发连接起来,并显著提高临床转化效率。
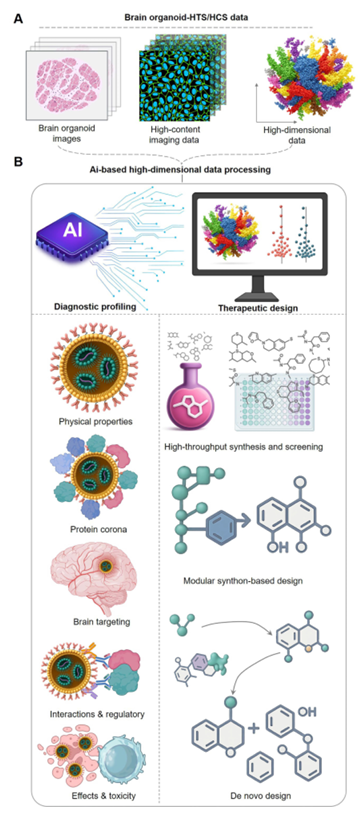
驱动治疗诊断工作流程的人工智能引擎。治疗诊断工作流程依赖于由脑类器官高通量/高内涵筛选平台生成的高维数据。这些数据作为诊断输入,由人工智能引擎处理,执行两个协同功能:
治疗诊断预测:AI模型经过训练,以预测纳米药物在体内复杂的行为。这包括预测其物理特性、蛋白质冠形成、脑靶向效率、与调节系统(如免疫细胞)的相互作用,以及整体疗效和毒性。这些预测为每个候选药物形成全面的诊断概况。治疗指导:基于诊断洞见,AI为新型和改良纳米治疗药物的设计提供合理的指导。这可能涉及高通量虚拟筛选、模块化合成基元设计,或新分子结构的从头设计。这个由AI引导的循环不断根据诊断预测优化治疗设计,加速发现有效且安全的脑靶向疗法。
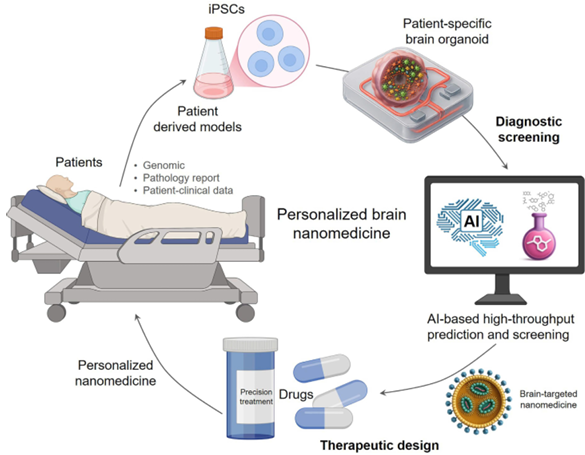
个性化脑部治疗诊断的拟议工作流程。此图展示了个体化患者护理的未来,由闭环治疗诊断工作流程实现。循环始于个体患者,从患者收集临床和生物数据(例如,基因组信息、病理报告)。这些信息用于构建“治疗诊断数字双胞胎”――一个患者特异性的脑类器官模型,能够再现个体的疾病。然后,将这一高保真模型置于基于人工智能的高通量筛选平台中,该平台执行两个关键任务:(1)‘诊断’类器官对一系列纳米药物的反应;(2)‘指导’最优个性化纳米疗法的合理设计。最后,将定制的纳米药物应用于患者,完成从诊断到精确治疗的以患者为中心的治疗诊断循环。
总结
脑部疾病因血脑屏障及复杂的生物机制,开发靶向治疗面临巨大挑战。传统药物研发模式效率低、成本高,且临床转化成功率不足。近年来,脑类器官与人工智能技术的结合,为脑靶向纳米药物研发带来新突破。脑类器官能高保真模拟人类大脑的复杂微环境,作为“诊断平台”为候选药物提供高效测试;人工智能则扮演“智能引擎”角色,通过处理高通量、高内涵的实验数据,进行药物行为预测与理性设计,形成“诊断―治疗―验证”的闭环研发体系,显著提升研发效率与靶向精度。该融合范式不仅加速了候选药物的发现与优化,更推动了个性化精准医疗的实现,为神经系统疾病的治疗带来了新的希望。
以患者来源的脑类器官与人工智能驱动的虚拟筛选、药物设计相结合,研发过程正从传统“线性流程”向“智能闭环”转变。这种整合不仅提升药物设计命中率,还可通过“数字孪生”模型预测患者个体对药物的反应,从而实现真正意义上的精准医疗。未来,随着类器官芯片、多组学技术及可解释人工智能的进一步发展,脑靶向纳米药物研发有望实现更高效率、更低成本、更个性化,为攻克阿尔茨海默病、脑肿瘤等难治性脑病开辟新的治疗路径。
参考文献:
DOI: 10.7150/thno.123243
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫