
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

细菌免疫疗法具有有前景的抗癌潜力。然而,要释放其力量,需要对细菌如何既能规避抗菌免疫防御,又能在肿瘤微环境中刺激抗肿瘤免疫反应的机制理解。在这里,通过利用一种工程化的沙门氏菌肠菌株,并具备这种双重能力,我们揭示了一个潜在的独特机制。具体来说,白介素-10 受体(IL-10R)的滞后非线性表达推动肿瘤浸润的免疫细胞进入肿瘤特异性的 IL-10Rhi 状态。细菌利用这一点增强产生 IL-10 的肿瘤相关巨噬细胞,避免肿瘤相关中性粒细胞的吞噬作用,同时同时扩增并刺激已耗尽的肿瘤驻留 CD8+ T 细胞。这种有效的组合能消除肿瘤,防止复发,并抑制多种肿瘤类型的转移。对人体样本的分析表明,IL-10Rhi 状态可能是人类肿瘤类型中普遍存在的特征。我们的研究揭示了细菌免疫疗法在实体肿瘤中面临双重挑战的未解机制,并为肿瘤内免疫调节提供了框架。
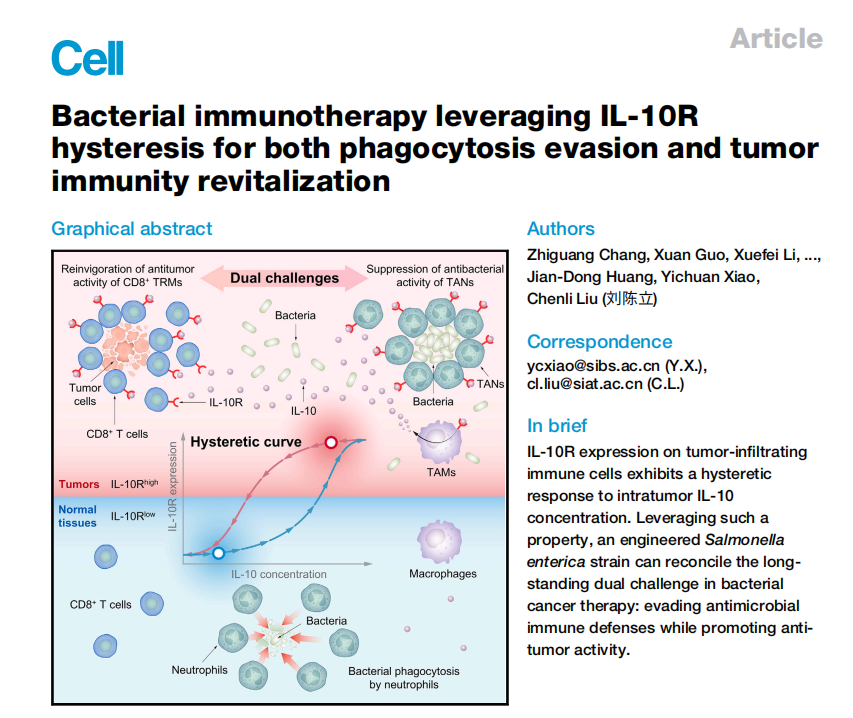
该研究以题为“Bacterial immunotherapy leveraging IL-10R hysteresis for both phagocytosis evasion and tumor immunity revitalization”发表在Cell上。
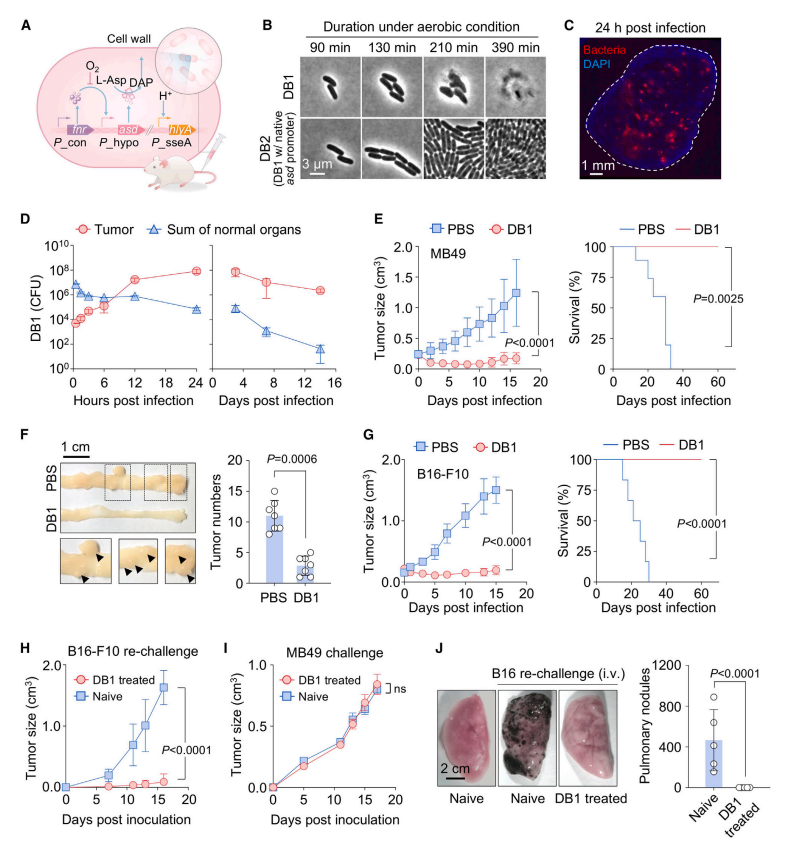
图1. DB1在实体瘤中选择性增殖并抑制其生长与复发 (A) DB1遗传回路示意图。P_con为组成型启动子;fnr为富马酸与硝酸还原转录因子;hlyA为编码 LLO 的基因;DAP为二氨基庚二酸。(B) 无DAP条件下有氧环境下的DB1与DB2延时显微照片。比例尺:3毫米。(C) DB1注射24小时后MB49肿瘤切片,采用抗沙门氏菌脂多糖抗体(红色)和 DAPI(蓝色)染色。比例尺:1毫米。(D) 通过定量分析DB1在MB49皮下肿瘤及正常器官(心脏、肝脏、脾脏、肺、肾脏和血液总和)中的集落形成单位(CFU),分别在10^7个DB1静脉注射后24小时和2周(n=3)。 CFU 值通过密度(每克 CFU 数)乘以组织重量计算,反映组织中细菌总载量。(E) 接受PBS或DB1处理的MB49荷瘤小鼠肿瘤生长曲线(左)与生存曲线(右)(n=6)。
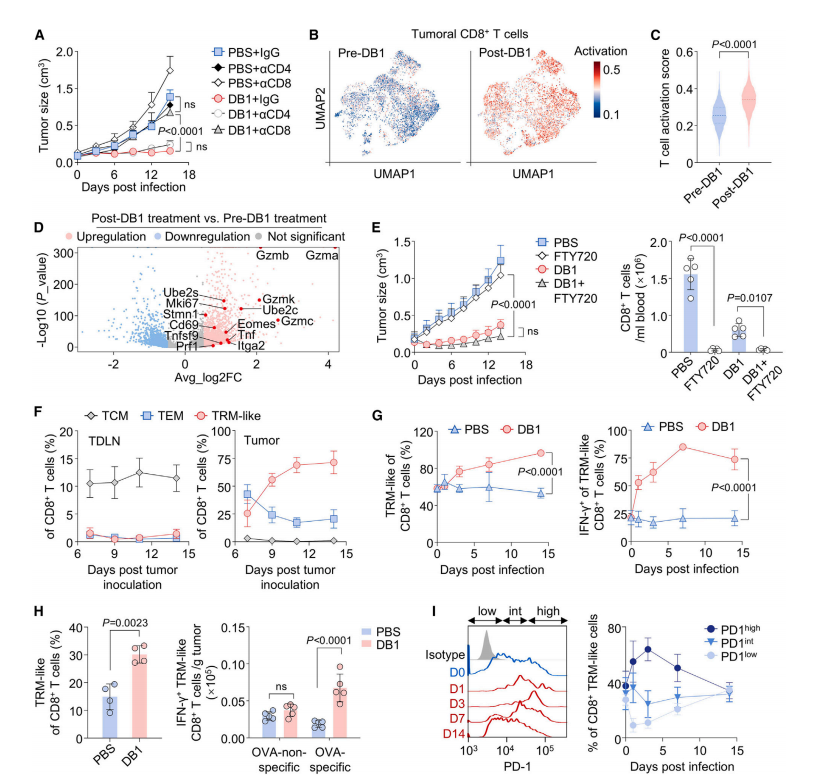
图2. DB1激活TRM样CD8+ T细胞并扩增PD-1+ TIM-3+ TRM样细胞 (A) 经PBS或DB1处理后,经抗体介导的CD8+ T细胞或CD4+ T细胞清除的MB49荷瘤小鼠肿瘤生长曲线(n=8-9)。(B) DB1处理前后MB49肿瘤中CD8+ T细胞的主成分分析,通过均匀流形近似与投影(UMAP)图呈现。 UMAP 图按T细胞活化评分着色;与T细胞活化相关的基因选自基因本体论术语T细胞活化(GO:0042110)。(C) 小提琴图显示CD8+ TILs的T细胞活化评分。(D) 火山图展示DB1处理前后组间CD8+ TILs的差异表达基因(DEGs)。DB1处理组中显著上调或下调的基因分别以红色和蓝色标示。(E)经PBS或DB1处理(联合或不联合FTY720治疗)的MB49荷瘤小鼠血液中肿瘤生长曲线(左)与CD8+ T细胞计数(右)(n=5-6)。(F)皮下接种MB49肿瘤细胞后,从小鼠腹股沟淋巴结(左)和肿瘤组织(右)分离的CD8+ T细胞中,TRM样(CD62L CD69+)、效应记忆(TEMs,CD69 CD62L CD44+)及中枢记忆(TCMs,CD69 CD62L+ CD44+)T细胞的百分比(n=6)。(G)经PBS或DB1处理后,MB49荷瘤小鼠肿瘤组织中CD8+ T细胞(左)及 IFN -γ分泌型TRM样CD8+ T细胞(右)中TRM样T细胞的百分比(n=5)。
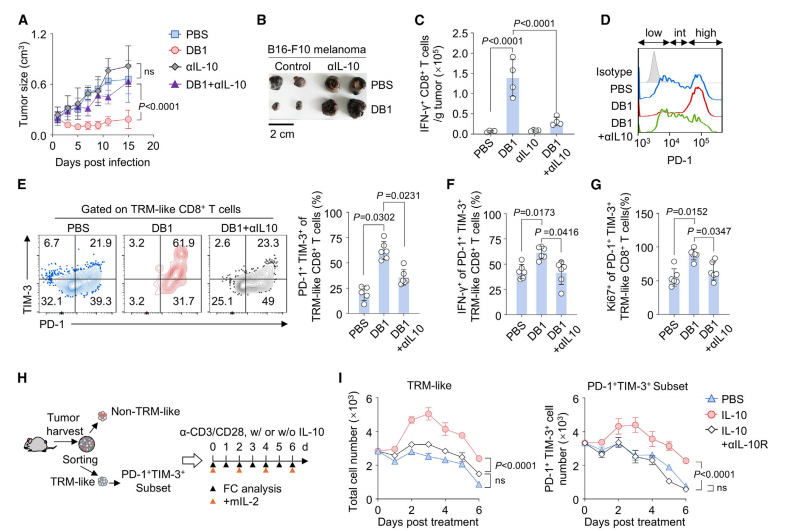
图3. DB1通过IL-10重新激活CD8+肿瘤浸润淋巴细胞(TILs)以抑制肿瘤生长 (A) 接受PBS、DB1、IL-10中和抗体(aIL-10)或DB1与aIL-10联合治疗的MB49荷瘤小鼠肿瘤生长曲线(n=5)。(B) 皮下接种B16-F10黑色素瘤荷瘤小鼠在给药后10天的肿瘤代表性照片(比例尺:2 cm)。(C) 接受PBS、DB1、aIL-10或DB1+aIL-10治疗的MB49荷瘤小鼠中 IFN -g+ CD8+ TILs的细胞计数(n=4)。(D) 给药3天后MB49荷瘤小鼠TRM样CD8+ TILs中PD-1表达的代表性流式细胞术直方图。(E) 给药3天后MB49荷瘤小鼠TRM样CD8+ TILs中PD-1+TIM-3+细胞的代表性流式细胞术图谱及百分比(n=5)。(F和G) 接受PBS、DB1或DB1与aIL-10联合治疗的MB49荷瘤小鼠中PD-1+TIM-3+ TRM样细胞中 IFN -g+(F)和Ki67+(G)的百分比(n=6)。(H) 体外分选TRM样CD8+ T细胞的实验设置。肿瘤接种后第14天从9至15只MB49荷瘤小鼠中收集CD8+ TILs,分别分选TRM样CD8+ T细胞和PD-1+TIM-3+ TRM样CD8+ T细胞亚群。每个亚群在a-CD3/CD28和小鼠IL-2(mIL-2)存在或不存在IL-10的条件下培养6天。(I)体外处理后TRM样CD8+ T(左)或PD-1+ TIM-3+ TRM样CD8+ T(右)亚群的细胞数量动态变化,处理条件包括PBS、20 ng/mL IL-10或IL-10与aIL-10R的组合(n=3)。数据以均值±标准差表示,来自至少三次生物学独立实验。统计分析采用双因素方差分析(A和I)和单因素方差分析(C和E-G)。
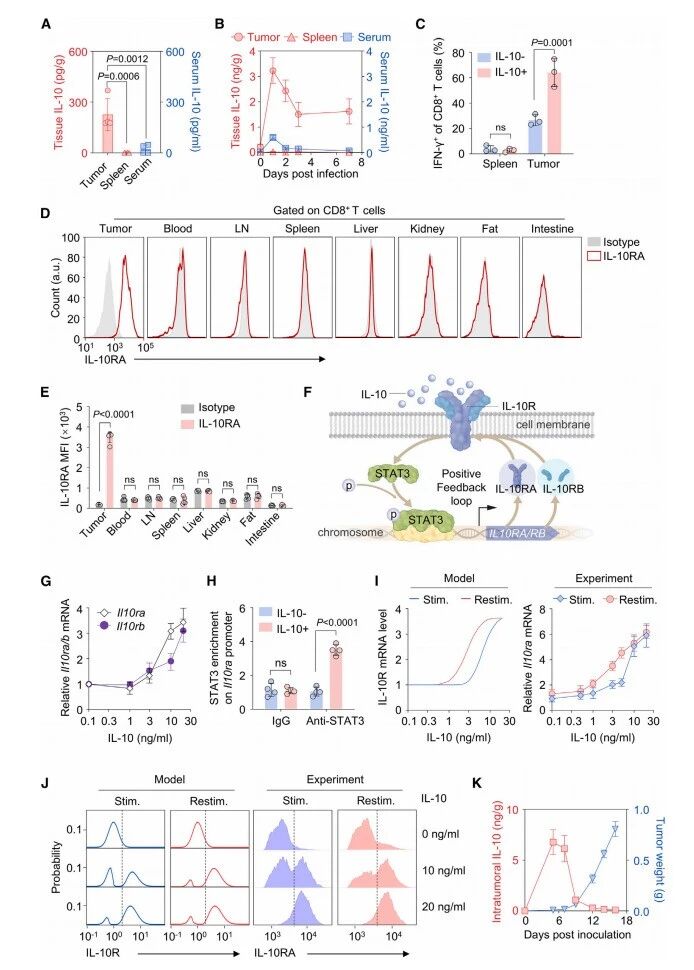
图4. CD8+ T细胞中IL-10R表达的滞后现象 (A) DB1治疗前(MB49肿瘤接种后第14天,n = 4)肿瘤、脾脏和血清中IL-10水平。(B) DB1治疗后IL-10浓度的变化趋势。左y轴:脾脏和肿瘤中的IL-10浓度。右y轴:血清中的IL-10水平。(C) 经10 ng/mL IL-10处理24小时后,脾脏或MB49肿瘤CD8+ T细胞中产生 IFN -g的CD8+ T细胞百分比。(D和E) MB49皮下荷瘤小鼠指定组织中CD8+ T细胞上IL-10RA表达水平的代表性流式细胞术直方图(D)和平均荧光强度(MFI)(E)。(F) IL-10/IL-10R/STAT3轴。示意图展示了IL-10诱导的STAT3激活,通过正反馈环促进IL10RA/IL10RB表达。(G) 经不同浓度IL-10刺激6小时后CD8+ T细胞中Il10ra和Il10rb mRNA表达水平(n = 3),以0.1 ng/mL IL-10处理条件为基准进行标准化。(H) 24小时IL-10刺激后CD8+ T细胞中STAT3在Il10ra启动子上的富集情况的ChIP-qPCR检测(n = 4)。(I) IL-10R滞后曲线。左:不同剂量IL-10刺激或再刺激后平均IL-10R mRNA水平的模型模拟。右:MB49荷瘤小鼠CD8+ TILs中Il10ra表达的qPCR分析,以初始0.1 ng/mL IL-10处理条件为基准进行标准化(n = 3)。(J) IL-10R表达的双峰分布。左图:IL-10R蛋白在刺激或再刺激后分布的模型模拟。右图:经指定处理后Jurkat T细胞上IL-10RA表达的流式细胞术分析。(K)皮下接种B16-F10黑色素瘤细胞后,瘤内IL-10水平与肿瘤大小的相关性(n=4)。数据以均值±标准差表示,来自至少三次生物学独立实验。统计分析采用单因素方差分析(A)和非配对双尾Student t检验(C、E和H)。
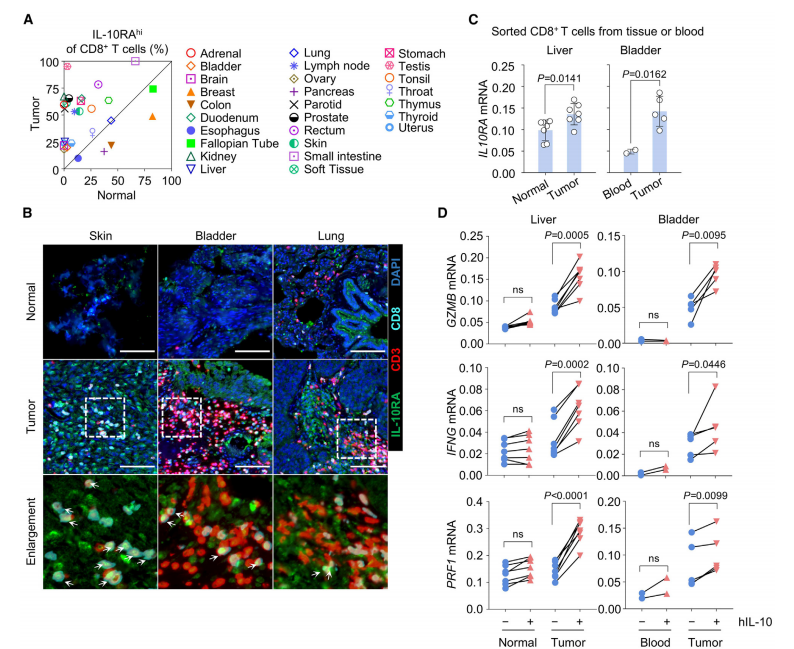
图5. CD8+ T细胞在多种人类肿瘤中高表达IL-10R,提示存在一种普遍的内在IL-10R滞后机制。(A) 27种人类肿瘤及其正常对照中CD8+ T细胞中IL-10RAhi细胞的频率。(B) 人类肿瘤及其正常对照的多重免疫组化染色代表性图像。CD3(红色)、CD8(青色)、IL-10RA(绿色)、 DAPI(蓝色),白色箭头指示IL-10RAhi CD8+ T细胞。比例尺:1毫米。(C) 从人类肿瘤组织、正常对照和外周血中分选的CD8+ T细胞的IL10RA mRNA水平的qPCR分析。(D) 体外分选的肝癌或膀胱癌患者CD8+ T细胞中 GZMB 、 IFNG 和PRF1 mRNA水平的qPCR分析,无论是否使用10 ng/mL人IL-10诱导。数据以均值±标准差表示,代表至少三次生物学独立实验。(C)和(D)显示归一化至 ACTB 的数据。患者详情见表S1。肝癌n=7;膀胱癌n=5。统计分析采用非配对双尾Student t检验(C)和配对双尾Student t检验(D)。
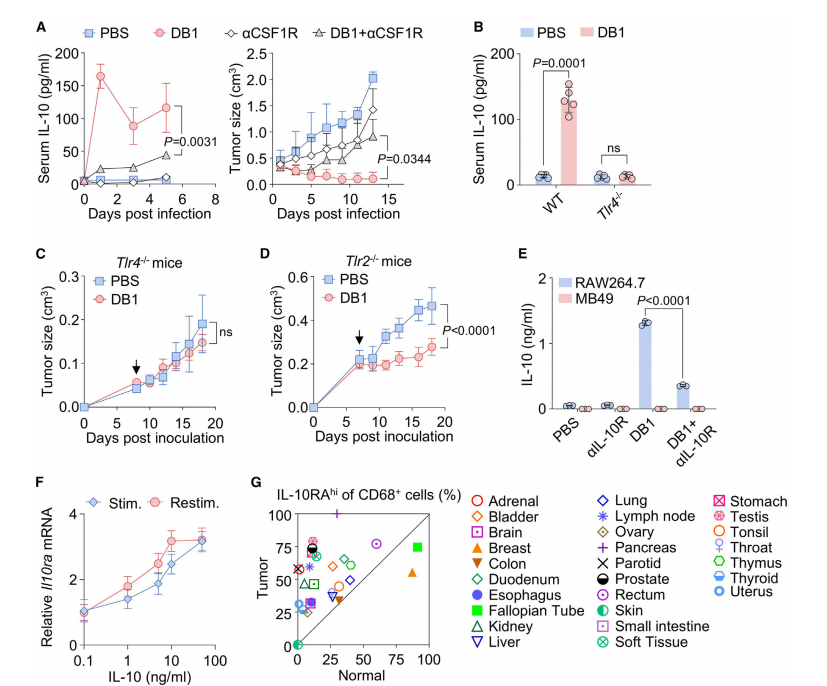
图6. DB1刺激的TAMs产生IL-10及TAMs中IL-10R滞后现象 (A) 经PBS、DB1、aCSF1R或DB1与aCSF1R联合处理的MB49荷瘤小鼠血清中IL-10水平(左)及肿瘤生长曲线(右)(n=5)。(B和C) (B) 野生型(WT)或Tlr4/骨髓重建受体小鼠经PBS或DB1处理后的血清IL-10水平及(C) B16黑色素瘤肿瘤生长曲线(B组n=5;C组n=3)。(D) 经WT或Tlr2/骨髓照射、接种B16-F10黑色素瘤并经PBS或DB1处理的小鼠肿瘤生长曲线(n=3)。(E) ELISA 分析RAW264.7巨噬细胞或MB49肿瘤细胞经指定处理后分泌的IL-10。(F) MB49荷瘤小鼠TAMs中Il10ra水平的qPCR分析,这些TAMs经不同浓度IL-10刺激或再刺激。数据以0.1 ng/mL IL-10组为基准进行标准化。(G) 27种人类肿瘤及其正常对照中CD68+细胞中IL-10RAhi细胞的频率。黑色箭头(C和D)标示DB1治疗开始时间(肿瘤接种后7天)。数据以均值±标准差表示,至少来自三次生物学独立实验。统计分析采用非配对双尾Student‘s t检验(B和E)及双因素方差分析(A、C和D)。
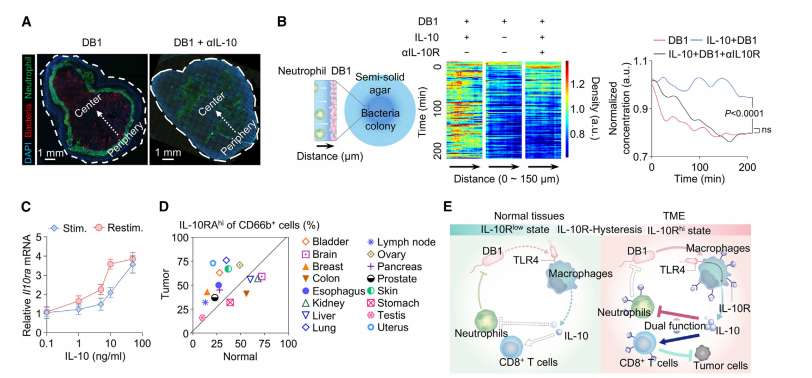
图7. TANs中IL-10R的滞后现象及中性粒细胞环的形成(A)来自MB49荷瘤小鼠经DB1或DB1联合aIL-10处理后的代表性免疫荧光图像。肿瘤切片经抗沙门氏菌LPS(红色)、抗Gr1(中性粒细胞,绿色)和 DAPI(蓝色)染色。比例尺:1毫米。(B)中性粒细胞运动性检测。展示在PBS、IL-10或IL-10联合aIL-10R存在下中性粒细胞密度的检测过程及时间动态变化。中性粒细胞密度分布根据距凝胶中心的距离进行估算。(C)MB49荷瘤小鼠肿瘤TANs中Il10ra水平的滞后分析,分别用不同浓度IL-10刺激或再刺激。数据以0.1 ng/mL IL-10组为基准进行标准化。(D)16种人类肿瘤及其正常对照中CD66b+中性粒细胞中IL-10RAhi细胞的频率。(E)正常与肿瘤组织间IL-10R水平差异的图示,受细胞因子瞬时波动及正反馈依赖性滞后特性影响。数据以均值±标准差表示,来自至少三次生物学独立实验。统计分析采用双因素方差分析(B)。
总结
一篇于2025年3月发表在《Cell》上的研究揭示了基于IL-10R滞回效应的细菌免疫疗法在实体瘤治疗中的新机制。研究团队通过改造一种鼠伤寒沙门氏菌,构建了可在肿瘤内特异性增殖的工程菌株DB1。该菌株通过携带氧气抑制型生长调控元件和溶素O基因,实现了在正常组织中被清除、在肿瘤内持续扩增的特性。研究发现,DB1在肿瘤内可诱导肿瘤相关巨噬细胞(TAMs)大量分泌IL-10,进而通过IL-10/IL-10R/STAT3正反馈通路激活肿瘤浸润的CD8+ T细胞,特别是PD-1+TIM-3+的衰竭型组织驻留记忆T细胞(TRM-like),显著增强其抗肿瘤活性。同时,IL-10还通过抑制肿瘤相关中性粒细胞(TANs)的趋化和吞噬功能,帮助细菌逃避宿主免疫清除,从而在肿瘤内形成免疫抑制与免疫激活并存的微环境。
进一步机制研究揭示,IL-10R在肿瘤浸润免疫细胞上的表达具有“滞回效应”(hysteresis),即细胞在经历高浓度IL-10刺激后,即使后续IL-10浓度下降,仍能维持较高水平的IL-10R表达。这一现象在CD8+ T细胞、TAMs和TANs中均被观察到,且依赖于STAT3与IL-10R启动子的结合。该机制使得肿瘤局部形成一种“免疫记忆样”状态,为细菌免疫疗法提供了独特的治疗窗口。研究还在多种人类肿瘤组织中验证了IL-10R高表达CD8+ T细胞的普遍存在,提示该机制具有跨物种和跨肿瘤类型的普适性。该研究不仅为细菌免疫疗法的“双重挑战”――即如何既逃逸抗菌免疫又激活抗肿瘤免疫――提供了统一机制解释,也为后续基于IL-10信号通路的免疫治疗策略提供了新思路。
参考文献:
DOI: 10.1016/j.cell.2025.02.002
 |
 |
 |
 |
| 二维材料Frontier | 生物纳米材料前沿 | MXenes Frontier | 纳米医学Frontier |
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |
扫一扫