
咨询热线:
17715390137
18101240246
18914047343
邮件:mxenes@163.com
扫码关注或微信搜索公众号:
二维材料Fronrier
关注后点击右下角联系我们,
进入企业微信。
专业服务在线

奇物论联合纳米人编辑部为大家整理了生物材料大佬、美国三院院士(“科学院院士”、“工程院院士”、“艺术与科学院院士”),麻省理工“David H. Koch学院教授”(MIT教授所能获得的最高荣誉)Robert S. Langer教授课题组2020年的部分研究成果。

Robert Langer教授是全球生物工程学领域的著名学者,尤其以对靶向药物输送系统和组织工程学的研究而知名,其在麻省理工的实验室目前是世界上最大的生物医学工程实验室(没有之一,且不接受反驳),作为生物材料领域第一大门派,该课题组已经实现了一流技术做产品,二流成果水CNS,三流产物扔顶刊。
他的课题组到目前为止已经发表1500多篇文章,还在全球拥有1400多个已发布和正在申请的专利。Langer教授的专利已被400多家制药,化学,生物技术和医疗设备公司许可或再许可。他是历史上被引用次数最多的工程师,H-index 280,被引量超过322,000。
Robert S. Langer教授课题组主要研究方向有:
1.聚合物释放机理的微观结构分析与数学模型研究
2.研究这些系统的应用,包括开发胰岛素、抗癌药物、生长因子、基因治疗剂和疫苗的有效长期输送系统
3.开发可通过磁性、超声波或酶促触发以提高释放速率的控释系统
4.合成新型生物可降解聚合物输送系统
5.创造新的方法来跨越诸如血脑屏障,肠,肺和皮肤等人体复杂障碍传递诸如蛋白质和基因之类的药物
6.研究创建组织和器官的新方法,包括为组织工程创建新的聚合物系统
7.干细胞研究,包括控制生长和分化
8.创造具有形状记忆或表面开关特性的新型生物材料
9.血管生成抑制
以下对Robert Langer研究团队2020年部分代表性研究成果进行归纳总结,供大家学习交流。(以通讯作者为主,如有疏漏,欢迎指正)
以下篇幅分三个部分展开
1. 药物递送
2. 口服递送
3. 技术优化
一、药物递送
1. Nature Reviews Drug Discovery: 工程化精准纳米颗粒用于药物递送(点击查看详细解读)
目前,许多科学家想要通过精准医学和个性化医学来克服NP的生物学障碍。基于在患者数据的基础上进行新的NP设计,可以大大改善精密药物治疗的递送和响应。
鉴于此,麻省理工学院Robert Langer院士、德州大学奥斯汀分校Nicholas A. Peppas院士和宾夕法尼亚大学Michael J. Mitchell等人在Nature ReviewsDrug Discovery上发表了用于药物递送的工程精准纳米颗粒的综述。他们集中于纳米医学的进展,这些进展可以促进精确药物的临床转化,并改善患者的治疗反应,重点是利用生物材料和生物医学工程创新来克服生物障碍和患者的异质性。
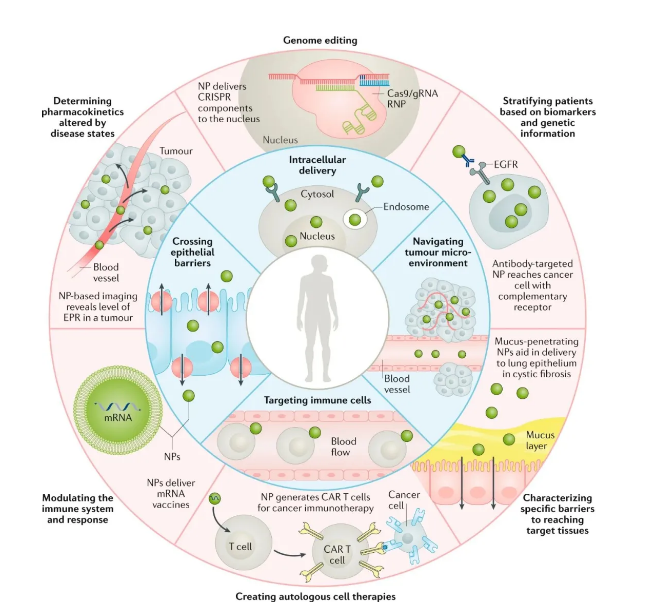
Mitchell, M.J., et al.Engineering precision nanoparticles for drug delivery. Nat Rev Drug Discov(2020).
https://doi.org/10.1038/s41573-020-0090-8
2. Science Translational Medicine:良“方”妙药只需一针,脉冲式释药实现有效治疗肿瘤!(点击查看详细解读)

在目前的临床试验中,STING激动剂的给药方案包括多次肿瘤内注射(例如,在28天的时间内进行三次注射,或者每9周一个治疗周期,每周一次注射),长达2年才能达到治疗目的功效。针打多了,而患者就不依从了。此外,多次肿瘤内注射将基于STING激动剂的治疗方法的范围限制为易于获得的肿瘤类型,并存在破坏肿瘤微环境(TME)和血管网络的风险,有可能促进癌细胞的外渗和转移。
麻省理工学院Robert Langer院士、Daniel G. Anderson和Ana Jaklenec等人通过将PLGA工程化为立方微粒,开发了一种多剂量药物输送平台。该平台可在不同的时间间隔释放一定剂量的STING激动剂,这样,单次注射或植入微粒即可提供完整的治疗过程。
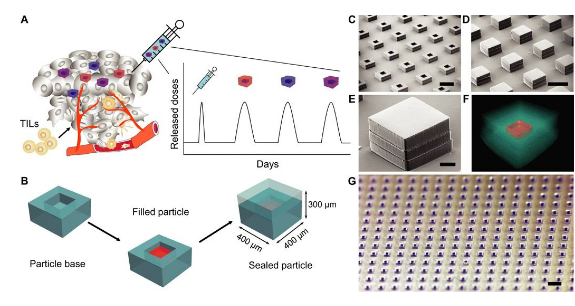
XueguangLu, et al., Engineered PLGA microparticles for long-term, pulsatile release ofSTING agonist for cancer immunotherapy. Science Translational Medicine 2020.
DOI:10.1126/scitranslmed.aaz6606
https://stm.sciencemag.org/content/12/556/eaaz6606
3. Advanced Drug Delivery Reviews: 高分子化学与免疫学的并行进化:机械生物学与材料设计的结合

Robert Langer等人讨论了临床上基于设备的和基于微/纳米颗粒的材料,以及对免疫系统如何与这些材料相互作用的生物学理解,这些不同的免疫细胞是如何成为药物递送设计的靶点和变量的,以及聚合物化学中解决这些相互作用的新方向,并进一步推动我们在医学治疗方面的进展。

Kaitlyn Sadtler, et al., Parallel evolution of polymer chemistry and immunology: Integrating mechanistic biology with materials design. Advanced Drug Delivery Reviews 2020.
https://doi.org/10.1016/j.addr.2020.06.021
4. Nano Lett:高分子纳米复合微致动器,用于通过高频磁场激发按需释放化学物质
在化学和生物医学工程领域,按需递送物质已被证明具有各种应用。先前已经显示了不同形状因数的微米/纳米颗粒的单脉冲释放曲线。然而,要获得持续释放,需要脉冲释放曲线。于此,麻省理工学院Robert Langer等人展示了载药聚合物磁性纳米复合微球的释放曲线。
通过用交流磁场激活微致动器,可以在五天内达到61%的累积释放。使用磁刺激的主要优点之一是,粒子所在环境的特性(例如透明度、密度和深度)不会影响性能。在这项工作中使用的磁场的工作幅度是安全的,不与任何非金属材料相互作用。该方法可应用于微化学、药物传递、芯片实验室和药物传递的微型机器人等领域。
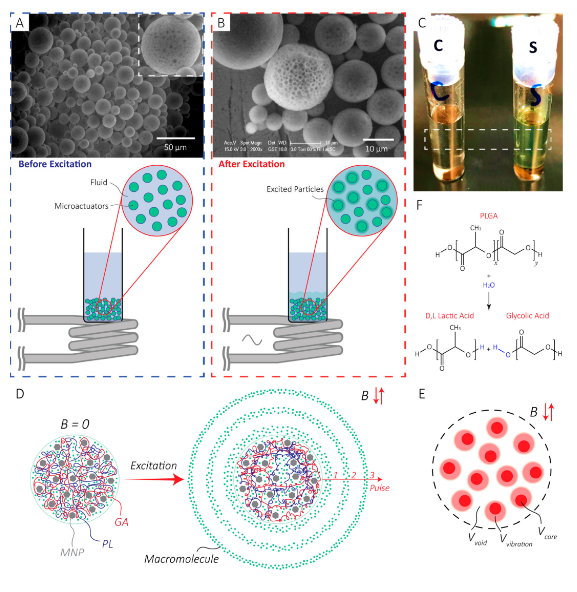
Seyed M. Mirvakili, et al., Polymer Nanocomposite Microactuators for On-Demand Chemical Release via High-Frequency Magnetic Field Excitation. Nano Letters 2020 20 (7), 4816-4822
DOI: 10.1021/acs.nanolett.0c00648
5.ACS Nano: 组织靶向递送手术刀:基于CRISPR/Cas的活体基因组编辑的机遇与挑战

基于CRISPR / Cas9的基因组编辑已迅速成为一项强大的突破性技术,可用于生物医学研究和治疗开发的多种环境。最近对了解体外基因修饰方法的努力已导致离体基因组编辑效率的显着提高。由于基因组校正的疾病靶标通常位于特定器官中,要实现基因组药物的全部潜能,就需要直接在体内递送靶向特定组织和细胞的CRISPR / Cas9系统。
于此,麻省理工学院Robert Langer等人专注于向体内递送CRISPR / Cas组分的进展。病毒和非病毒递送系统都有望通过局部注射和全身注射在多种组织中进行基因编辑。他们描述了用于体内基因编辑以及在研究和治疗模型中的应用的各种病毒载体和合成非病毒材料,并总结了迄今为止这两种方法的机会和进展。还将讨论病毒传递的挑战,包括克服有限的包装能力,与多次给药相关的免疫原性,脱靶效应的潜力以及非病毒传递,包括努力提高功效和扩大非病毒载体在肝外组织中的应用和癌症。展望未来,将需要在用于组织和细胞类型特异性基因编辑的病毒和非病毒递送系统的安全性和效率方面取得其他进步,以实现广泛的临床翻译。还提供了用于体内基因组编辑的当前递送系统的摘要,并按给药途径进行了组织,并重点介绍了生物医学研究和应用的直接机遇。此外,讨论了体内递送CRISPR / Cas9系统的当前挑战,以指导未来疗法的发展。
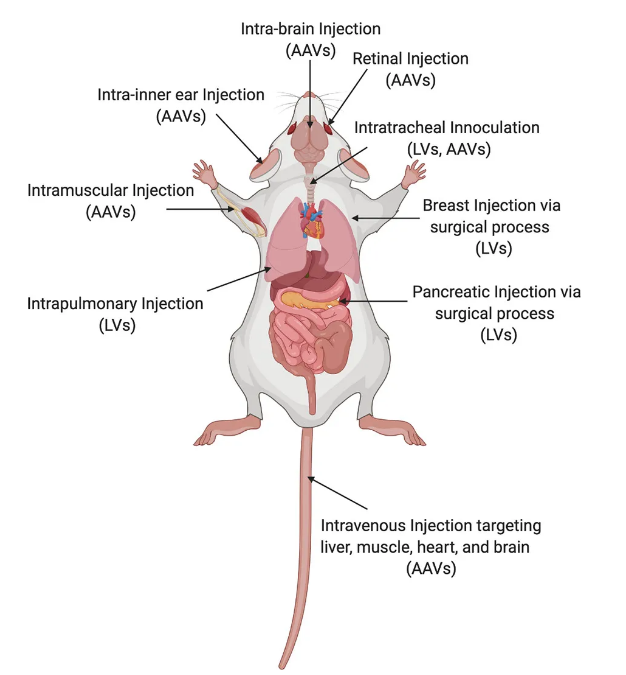
Tuo Wei, et al., Delivery of Tissue-Targeted Scalpels: Opportunities and Challenges for In Vivo CRISPR/Cas-Based Genome Editing. ACS Nano 2020 14 (8), 9243-9262
DOI: 10.1021/acsnano.0c04707
此外,还有Robert Langer教授作为共同作者的部分研究成果:



二、口服材料
6. PNAS:开发用于猪丙型肝炎病毒的长效直接作用抗病毒系统

直接作用抗病毒(DAA)治疗对丙型肝炎病毒(HCV)是非常有效的。尽管如此,慢性丙肝的负担仍然很高,特别是在那些每天服用药物都很困难的人群中。因此,产生长效的DAA传递模式可以扩大HCV的治疗。
麻省理工大学Daniel G. Anderson、Robert Langer等人开发了一种长效DAA系统(LA-DAAS),它可以支持HCV-DAAS的数克级药物库,并在数周内提供这些药物的控制释放。在猪模型上证明了LA-DAAS的初步安全性和有效性。扩大DAA向患者和医疗保健提供者的递送范围,将进一步致力于在全球范围内消除HCV感染。
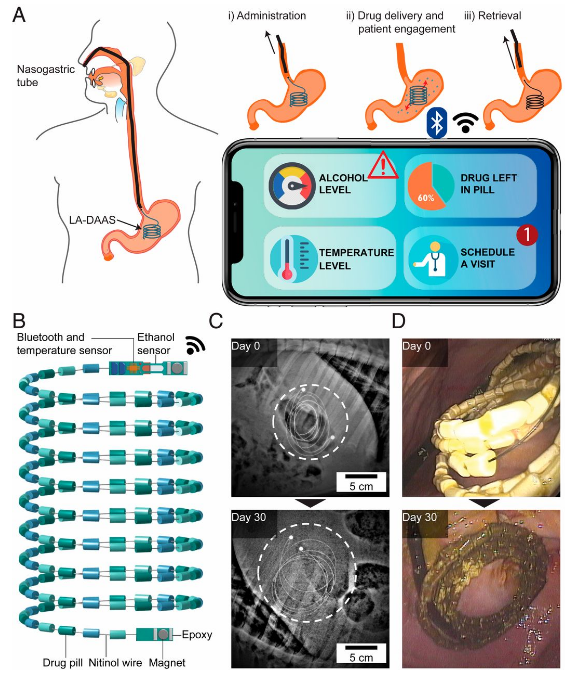
Malvika Verma, et al., Development of a long-acting direct-acting antiviral system for hepatitis C virus treatment in swine. PNAS 2020.
https://www.pnas.org/content/117/22/11987.short
7. Science Advances: 用于微刺激和传导信号的可吸收瞬态锚定电子设备

可摄取的电子设备能够对胃肠道(GI)进行无创评估和病理诊断,但通常无法与组织壁进行治疗性相互作用。于此,麻省理工学院Giovanni Traverso和Robert Langer院士等人开发了一种口服电刺激装置,其特征是在离体人体组织和在体猪模型中,通过自主插入导电钩状探针将自身瞬时固定在胃上。
探针通过定时电脉冲向组织提供刺激,可以用作治疗胃动力障碍的方法。为了证明与胃肌肉组织的相互作用,研究人员使用电刺激来诱发急性肌肉收缩。脉冲将探针的成功锚固和脱离事件传导到肠胃外放置的设备。锚固到由肠神经系统控制的目标胃肠组织中并与之交互作用的能力为治疗多种相关的病理学提供了机会。
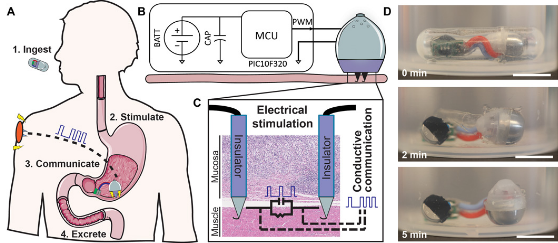
Alex Abramson, et al., Ingestible transiently anchoring electronics for microstimulation and conductive signaling. Science Advances 2020.
DOI: 10.1126/sciadv.aaz0127

三、技术优化
8. Nature Biomed. Eng.: 自动全组织培养系统,用于筛选口服药物制剂

单层癌细胞株被广泛应用于药物胃肠道吸收的模拟和口服药物的开发。然而,它们通常不能预测药物在体内的吸收。于此,麻省理工学院Giovanni Traverso和Robert Langer院士等人报道了一个机器人操作系统,它使用大的猪胃肠道组织外植体,这些外植体在培养中的功能保持了较长的时间,以便对胃肠道的整个部分进行高通量询问(每天数千个样本)。
本文要点:
1)与Caco-2 Transwell系统(斯皮尔曼相关系数分别为0.906和0.302)相比,自动培养系统在人类胃肠道中的药物吸收预测性更高。
2)通过使用培养系统分析2930种缩氨酸药物催产素制剂的肠道吸收,研究人员发现了一种吸收促进剂,在没有肠组织细胞破坏的情况下,可使猪口服催产素的生物利用度增加11.3倍。机器人操作的全组织培养系统应该有助于促进口服药物制剂的发展,也可能有助于药物筛选应用。
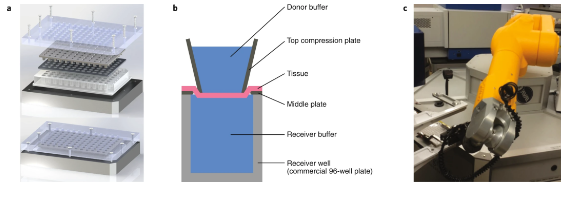
von Erlach, T., et al. Robotically handled whole-tissue culture system for the screening of oral drug formulations. Nat Biomed Eng (2020).
https://doi.org/10.1038/s41551-020-0545-6
9. Science Advances:优化微粒药物制剂的注射性(点击查看深度解读)

受注射微粒(特别是大微粒)的挑战与启发,麻省理工学院Ana Jaklenec和Robert Langer院士等人系统地研究微粒通过皮下注射针头的输送。研究人员现在已经开发出一种计算模型,可以帮助他们改善此类微粒的可注射性并防止堵塞。该模型分析各种因素,包括颗粒的大小和形状,以确定可注射性的最佳设计。使用该模型,研究人员能够成功注射的微粒百分比增加了六倍。他们现在希望使用该模型来开发和测试可用于递送癌症免疫治疗药物的微粒,以及其他潜在应用。
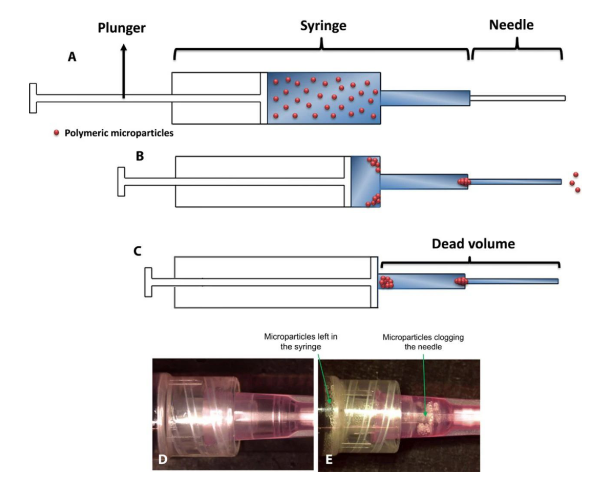
MortezaSarmadi, et al., Modeling, design, and machine learning-based framework foroptimal injectability of microparticle-based drug formulations. ScienceAdvances 2020.
DOI:10.1126/sciadv.abb6594
https://advances.sciencemag.org/content/6/28/eabb6594

此外,该课题组还有一些研究成果,由于篇幅关系,就不在此一一列举,感兴趣的读者可自行去课题组网站学习。
课题组网站:https://langerlab.mit.edu/
|
版权所有 © 2019 北京北科新材科技有限公司
All rights reserved. 京ICP备16054715号-2 |