��������AG����ƽ̨����521006914Q
QQѧ������Ⱥ��1092348845
��ϸ����
����Ա����QQͬ��521006914���ٷ���վ��www.TL9043.com���������ʿͷ�24Сʱ����,����˾ֱ���ͷ�������˾ֱ����������������ǡ�֧����Ƶ��֤�ֳ���
����ø��һ����иߴ�Ч�ʺ��ȶ��Ե�����ģ��ø����ҽ�����ײ���������й�����Ӧ��ǰ������������ѧ���ij´�Ӣ��������귢չ��һϵ�о��ж�����������Ե�����ø������һ����ϸ���Ͷ��������֤������ø���ԣ���سɹ���2020��ֱ�����Gold Nanorod-Based Nanoplatform Catalyzes Constant NO Generation and Protects from Cardiovascular Injury��, ��Graphdiyne-Templated Palladium-Nanoparticle Assembly as a Robust Oxygen Generator to Attenuate Tumor Hypoxia������Defect�\Rich Adhesive Molybdenum Disulfide/rGO Vertical Heterostructures with Enhanced Nanozyme Activity for Smart Bacterial Killing Application��Ϊ�ⷢ����ACS Nano��Nano Today��Advanced Materials�ڿ��ϡ�
01
ͬʱ����NADPH����ø��SODø��NOSø���Ե�����ø������Ѫ�ܼ�������
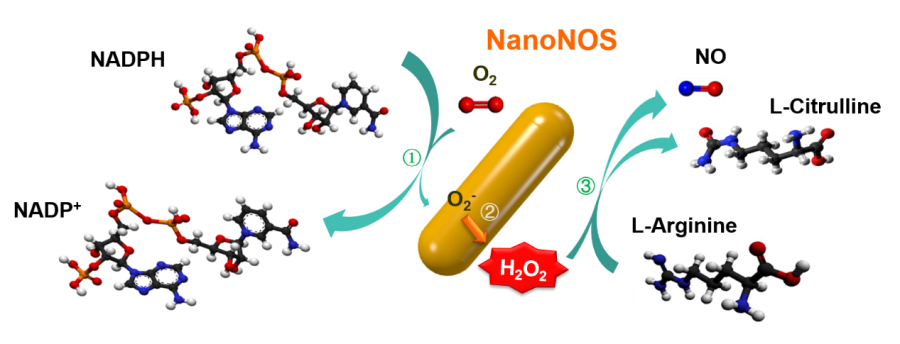
ͼ1. NanoNOS�Ĵ�����
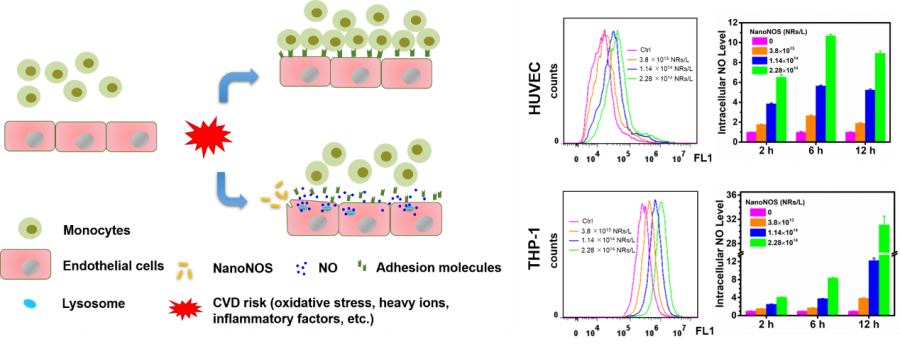
ͼ2. NanoNOS������Ƥ����ʾ��ͼ��ϸ����NOˮƽ��NanoNOS��Ũ�Ⱥͱ�¶ʱ��������
02
ʯīȲ��ά�����ϲ���ģ���������ø���ڷ�����������

ͼ3. PdNPs/GDY�ĺϳɼ��仯ѧ�ṹ
�������У�GDY����ͨ�����Ӵ���ά��Pdԭ�ӵĵͼ�̬���Ӷ����ֳ������ĸߴ����ԡ�����ϸ��ʵ���벡����Դ������ֲС��ģ�ͣ�PDX��ʵ��֤����PdNPs/GDY�ܹ���Ч�������طֽ�������ԴH2O2�����������������ظ��������������µ������յ�����(HIF-1��)�鵼������Ѫ���������Ӷ���������������������PdNPs/GDY��������������뻯��ҩ��DOXͬʱ���ƣ�����ʵ�ֻ�ѧ-���������ƣ��ܹ���Ч�����������������ﵽ��������Ŀ�ģ�ͼ4�������о�Ϊ���ͷ����������������ײ��ϵ���ƺ��Ż��ṩ����˼·��
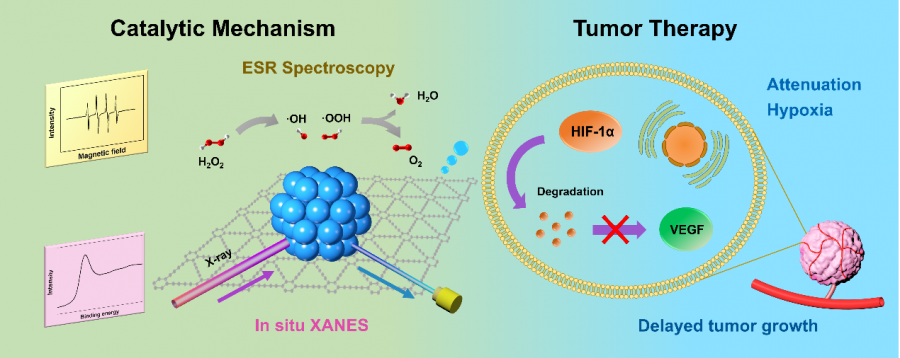
ͼ4. PdNPs/GDY��ø�������о���������������
03
������һ����ø�����Ե�MoS2/rGO��ֱ���ʽṹ������ҩϸ����Ⱦ����

ͼ5. �ٲ�MoS2����Ƭ��ֱ������rGO�ı��棬��¶�˸���ı�Ե����λ�㣬ͬʱ�γ��˴�����Mo��λ��S��λ

ͼ6. ��a-b������ǿ��������ø���ԡ���c����ֱ���ʽṹ�ֲڱ�����������ò���ϸ��
�ο����ף�[1]Li, H.; Yan, J.; Meng, D.; Cai, R.; Gao, X.; Ji, Y.; Wang, L.; Chen, C.; Wu, X., Gold Nanorod-Based Nanoplatform Catalyzes Constant NO Generation and Protects from Cardiovascular Injury. ACS Nano 2020, 14 (10), 12854-12865.
[2]Liu, J.; Wang, L.; Shen, X.; Gao, X.; Chen, Y.; Liu, H.; Liu, Y.; Yin, D.; Liu, Y.; Xu, W.; Cai, R.; You, M.; Guo, M.; Wang, Y.; Li, J.; Li, Y.; Chen, C., Graphdiyne-templated palladium-nanoparticle assembly as a robust oxygen generator to attenuate tumor hypoxia. Nano Today 2020. doi: 10.1016/j.nantod.2020.100907
[3]Wang, L.; Gao, F.; Wang, A.; Chen, X.; Li, H.; Zhang, X.; Zheng, H.; Ji, R.; Li, B.; Yu, X.; Liu, J.; Gu, Z.; Chen, F.; Chen, C., Defect-Rich Adhesive Molybdenum Disulfide/rGO Vertical Heterostructures with Enhanced Nanozyme Activity for Smart Bacterial Killing Application. Adv. Mater. 2020. doi: 10.1002/adma.202005423
��Ϣ��Դ:����ø
����ϢԴ�Ի���������ѧ������ ������Ȩ����ϵ��������ɾ��

 ѧ��ǰ��
ѧ��ǰ��
