用于治疗肺癌的载药可注射热致凝胶
QQ学术交流群:1092348845
详细介绍
厄洛替尼(ERT)是一种治疗肺癌的热门药物。目前,ERT仅在市场上以薄膜包衣片的形式提供。然而,因具有强的疏水性,口服ERT的药物吸收率低,需要大剂量给药,由此产生一系列的副作用,如:皮疹、腹泻、眼部损伤和胃肠道穿孔等。基于水凝胶的原位药物递送系统可实现患处精准药物释放,减小了给药剂量,极大提高药物利用率。但水凝胶是水性体系,疏水药物难以与之均匀混合,这导致药物负载量及释放速率难以控制。
1. 中空介孔二氧化硅载药纳米胶囊作者基于改进的Stöber方法合成了二氧化硅纳米粒子。然后用表面活性剂模板溶胶-凝胶法将介孔二氧化硅壳包被在二氧化硅核上。最后通过化学刻蚀方法除去颗粒核以形成中空结构(图2a)。
2. 热致凝胶的药物缓释在这项研究中,基于中心PEG嵌段和末端PDLLA嵌段的胶束水凝胶表现出可逆的温度依赖性溶胶-凝胶-溶胶转变。如图3A所示,随着温度的升高,所得的水凝胶复合材料经历了溶胶和凝胶的物理状态。
载药HMSNs粒子可以在室温下通过适当比例的简单混合轻松掺入水凝胶中,从而获得了均质且自由流动的HMSNs / PLEL可注射水凝胶负。ERT分别为2mg/mL和6 mg/mL的两种HMSN 凝胶样品均可以在37°C下保持无流动条件,这表明其在体温下的凝胶行为。
图3C展示了药物累积释放曲线。结果显示:在最初的72小时内,HMSNs和HMSNs/gel组分释放了39%和24%的ERT,显著低于游离ERT组。
3. 体内抗肿瘤效率研究人员用不同的ERT配方治疗肺癌裸鼠模型。根据肿瘤图像(图 4A)和肿瘤生长曲线(图 4B)结果显示:口服ERT、局部可注射的ERT @ HMSN和ERT @ HMSN /凝胶均显示出对A549肿瘤发展的有效抑制。
与ERT @ HMSNs及口服组相比,ERT @ HMSNs / gel(50 mg kg -1)可以进一步显著增强抗肿瘤效果,在第21天的肿瘤体积百分数为30.3%(p <0.01)。ERT的优化递送系统可以用相对低的剂量显着提高治疗效果。此外,对于凝胶组,当HMSNs /水凝胶系统中的ERT剂量增加到50 mg kg-1或100 mg kg -1时,肿瘤的快速生长几乎被完全抑制,这表明凝胶中的ERT可以剂量依赖的方式改善治疗效果。
为了解决以上问题,来自四川大学的钱志勇教授团队开发出一种基于聚丙交酯-聚乙二醇-聚丙交酯(PDLLA-PEG-PDLLA)胶束的温敏可注射水凝胶(PLEL水凝胶)。通过将包载厄洛替尼的中空介孔二氧化硅(HMSN)复合入该凝胶体系,实现了药物的可控释放。相关研究论文:Injectable Thermosensitive Hydrogel Containing Erlotinib-Loaded Hollow Mesoporous Silica Nanoparticles as a Localized Drug Delivery System for NSCLC Therapy 发表于杂志Advanced Science上。
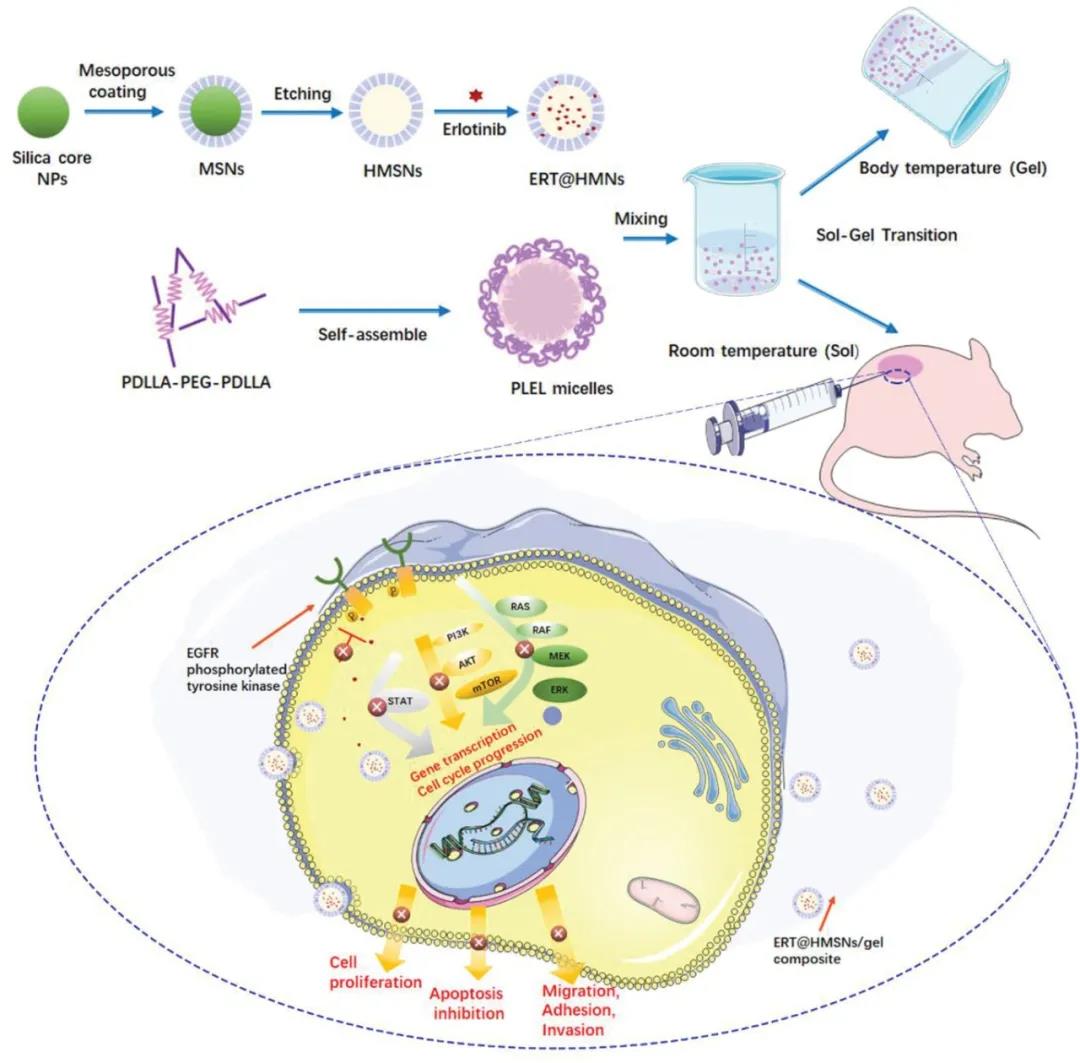
图1 载药可注射热致凝胶方案示意图
1. 中空介孔二氧化硅载药纳米胶囊作者基于改进的Stöber方法合成了二氧化硅纳米粒子。然后用表面活性剂模板溶胶-凝胶法将介孔二氧化硅壳包被在二氧化硅核上。最后通过化学刻蚀方法除去颗粒核以形成中空结构(图2a)。
药物的负载是通过溶剂蒸发法实现的。因为所制备的纳米胶囊具有空心结构,最终药物的负载率高达45%,远高于普通介孔二氧化硅纳米粒子。
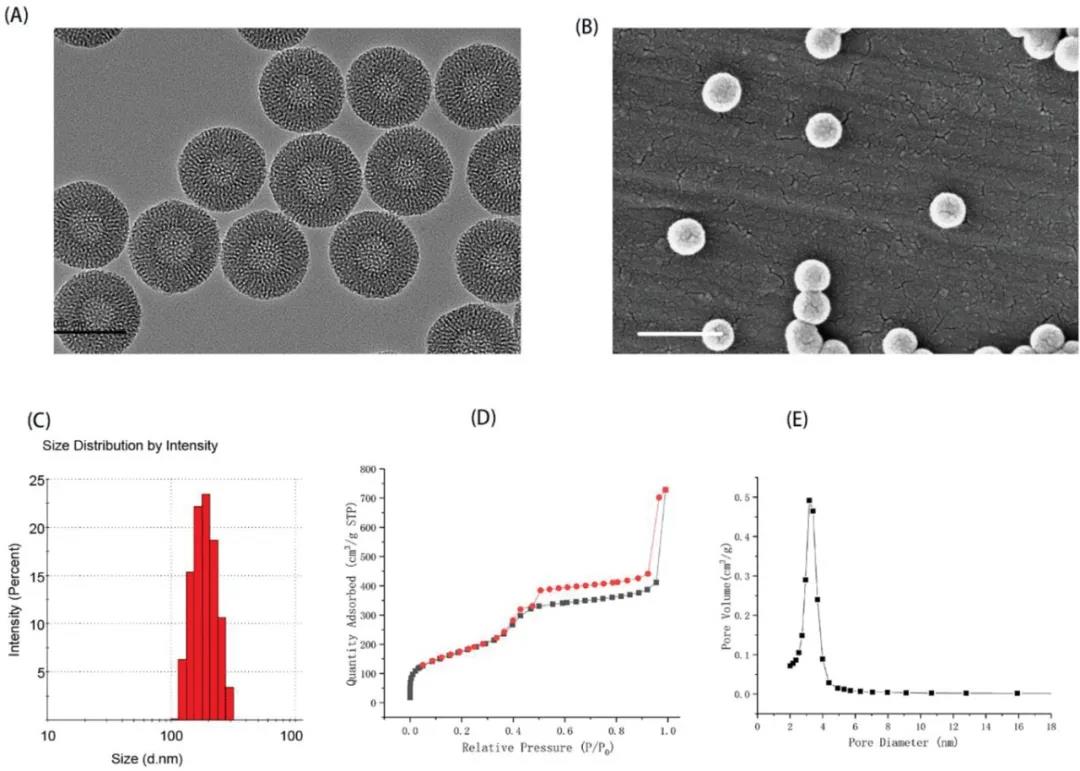
图2 中空介孔二氧化硅纳米粒子TEM、SEM、粒径、比表面积表征
2. 热致凝胶的药物缓释在这项研究中,基于中心PEG嵌段和末端PDLLA嵌段的胶束水凝胶表现出可逆的温度依赖性溶胶-凝胶-溶胶转变。如图3A所示,随着温度的升高,所得的水凝胶复合材料经历了溶胶和凝胶的物理状态。
载药HMSNs粒子可以在室温下通过适当比例的简单混合轻松掺入水凝胶中,从而获得了均质且自由流动的HMSNs / PLEL可注射水凝胶负。ERT分别为2mg/mL和6 mg/mL的两种HMSN 凝胶样品均可以在37°C下保持无流动条件,这表明其在体温下的凝胶行为。
图3C展示了药物累积释放曲线。结果显示:在最初的72小时内,HMSNs和HMSNs/gel组分释放了39%和24%的ERT,显著低于游离ERT组。
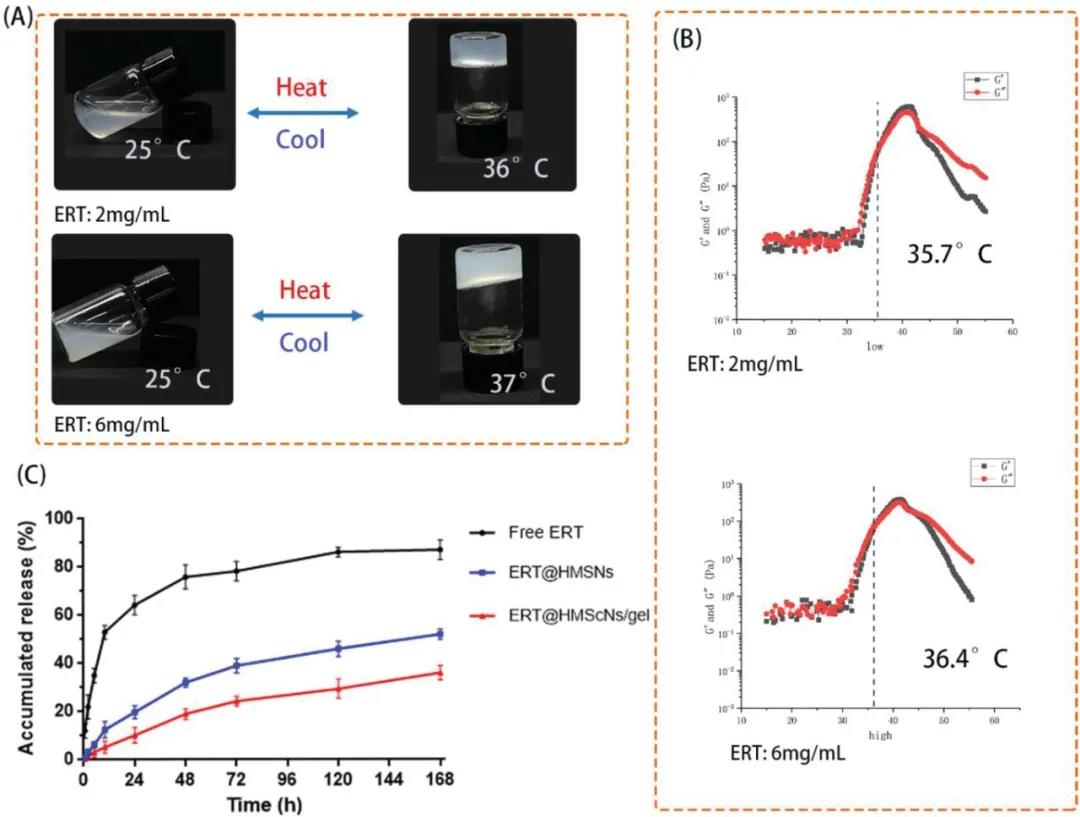
图3 载药热致水凝胶的凝胶化过程及药物释放表征
3. 体内抗肿瘤效率研究人员用不同的ERT配方治疗肺癌裸鼠模型。根据肿瘤图像(图 4A)和肿瘤生长曲线(图 4B)结果显示:口服ERT、局部可注射的ERT @ HMSN和ERT @ HMSN /凝胶均显示出对A549肿瘤发展的有效抑制。
与ERT @ HMSNs及口服组相比,ERT @ HMSNs / gel(50 mg kg -1)可以进一步显著增强抗肿瘤效果,在第21天的肿瘤体积百分数为30.3%(p <0.01)。ERT的优化递送系统可以用相对低的剂量显着提高治疗效果。此外,对于凝胶组,当HMSNs /水凝胶系统中的ERT剂量增加到50 mg kg-1或100 mg kg -1时,肿瘤的快速生长几乎被完全抑制,这表明凝胶中的ERT可以剂量依赖的方式改善治疗效果。
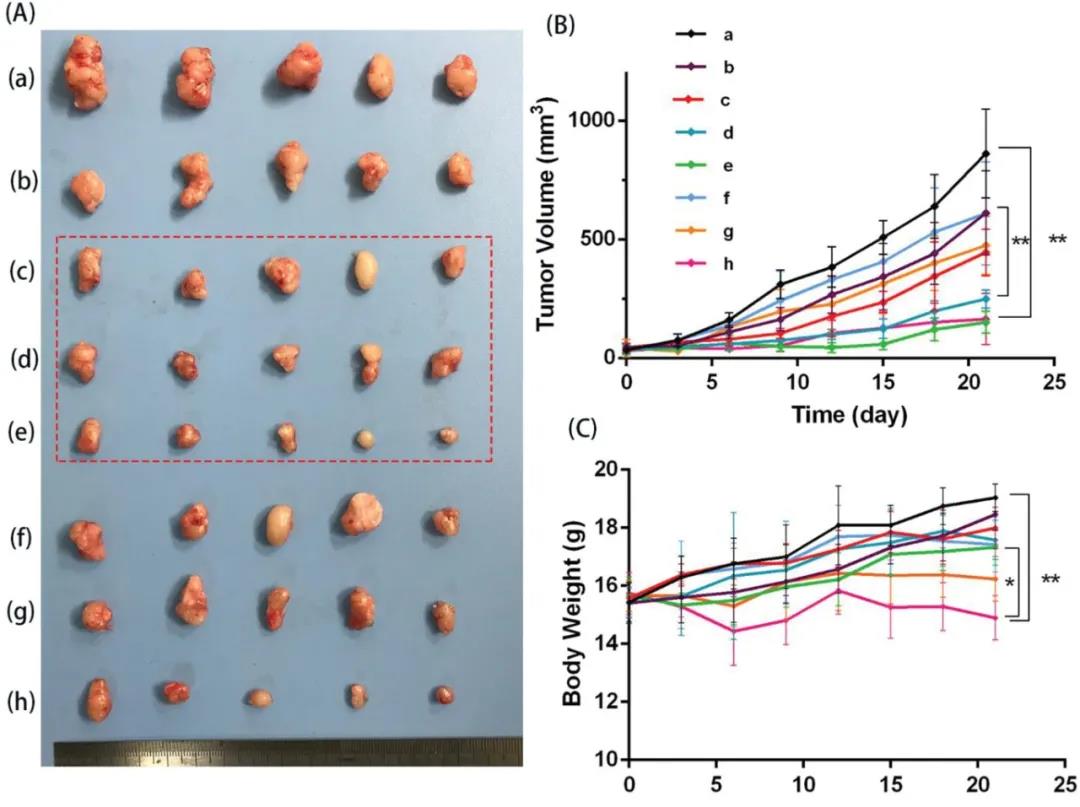
图4 A)每组皮下肿瘤的照片:a)空白;b)载药纳米胶囊(50mg/kg); c,d,e)载药凝胶(25,50,100mg/kg);f,g,h)口服ERT(每天25,50,100mg/kg)B)各组的肿瘤生长曲线。C)每组中小鼠的体重随时间的变化。
该研究设计了一种基于三嵌段聚合物的温敏热致可注射水凝胶,以其作为疏水抗肿瘤药物的负载控释平台。为了提高疏水药物的负载量及在水凝胶中的分散性,研究人员制备了一种中空介孔二氧化硅,将药物负载量提高至45%。此原位固化热致水凝胶可控制药物释放。体内实验结果显示在更低给药剂量下,与口服药物相比,该药物控释体系呈现出更好的肿瘤生长抑制作用。- 上一款: 北京化工大学徐斌、朱奇珍《AFM》:MXen
- 下一款: 《Nature》| MXene重大突破:纳米

 mxene 学术专题
mxene 学术专题
