
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

��������ȫ���������ϸ������Ĥ�����Ĵ����в�����������ϸ�����Ի�������ROS������֯�ܻ��ʽ�������ø��MMPs���Ļ��ۣ������������ƻ���Ŀǰ�����Ʒ�����������ϲ�ȷ������Ĥ��������ȫ�Լ���֯�������㡣ΪӦ����Щ��ս�������һ�ֿ�ע��������� Ce6@PEG MoO x -����ˮ������ͨ�����ṹʵ�֣��������ܱջ���ʵ��ȫ������������ע�������Ҵ���ˮ������������֯����Ӧ���� MMPs��ʵ�ְ���������ͷš�ͨ�����ɹ�������ˮ�����ٽ��˶������ܴ���ȵķ������ԡ���ȷ�ҿ��ظ��IJ������Ӷ�ʵ����������Ϻͼ�⡣����ͷŵĸ���������λ�� MoO������ø����ϸ������Ӧ��������������ǿ Ce6 �鵼�Ĺ��ѧ�����������Ĥ������ɱ�����̺���������� ROS��ֵ��ע����ǣ���ϵͳ�����˷ǰе� ROS �����������ˣ������˰����������ڵ���Χ��֯�����չ�ֳ�Խ�Ĺ�� ROS �������������⣬�ͷŵ� Mo ���� PI3K/AKT ͨ·���ϵ�Ѫ���������ӣ��ر�� M2 ����ϸ���ļ��������̼����ܸ�ϸ���ijɹǡ�������ԣ���һ������Ӧ��̬ϵͳ��������ϡ���⡢����Ĥ�崴����֯�����������˾��������ٴ�DZ���ıջ������ơ�

���о�����Ϊ��ASelf-Adaptive Periodontal Ecosystem Engineered With Molybdenum-Based Nanozyme-EmbeddedComposite Hydrogel for Microenvironment-Responsive Precision Therapy��������Advanced Materials�ϡ�
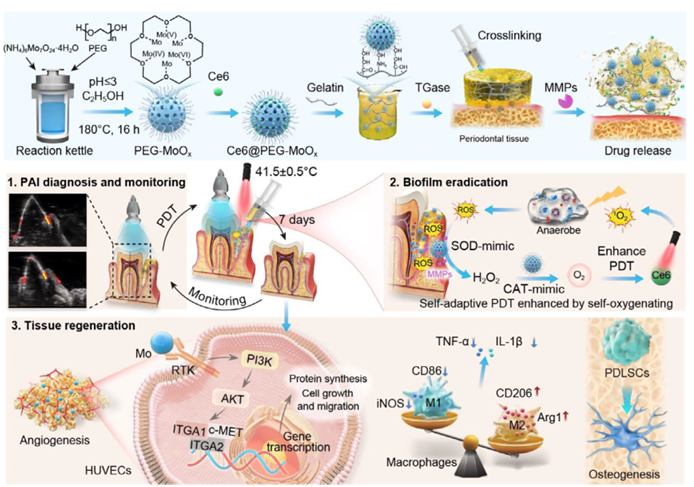
����Ӧ���� Ce6@PEG-MoOx TG-������̬ϵͳ�����������еĹ���ʾ��ͼ���������������ָ������TG ָ�ںϳɹ�����ʹ�õ�ת�Ȱ�����ø
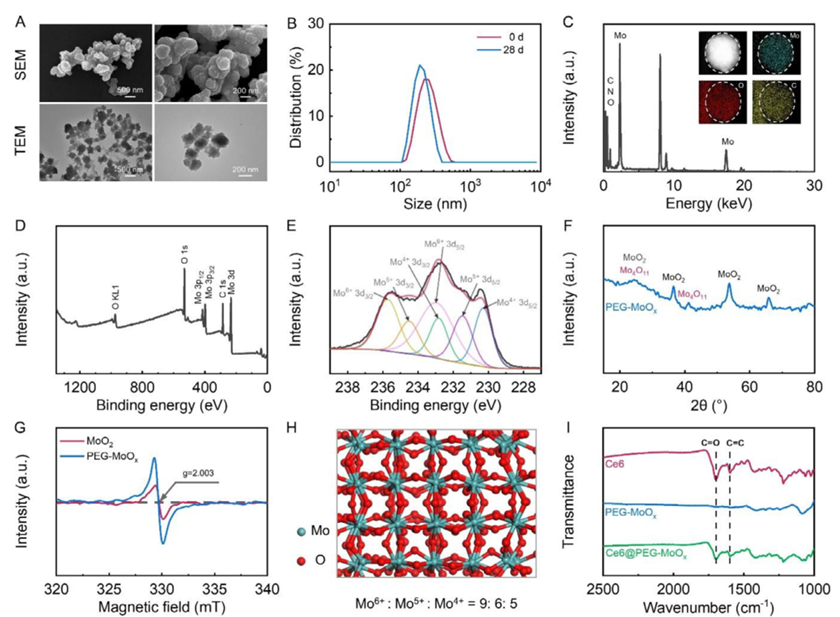
PEG-MoOx �� Ce6@PEG-MoOx �ı�����(A) PEG-MoOx ��������NPs����ɨ�����������SEM���������������TEM��ͼ��(B) ͨ����̬��ɢ�䣨DLS����õ� PEG-MoOx NPs �ߴ�ֲ���(C) ����ɫɢ�ף�EDS������� (D) PEG-MoOx �� X ���߹�������ף�XPS�������(E) XPS �߷ֱ�ɨ������ʾ PEG-MoOx �� Mo ���ڶ��ּ�̬��Mo4��Mo5 �� Mo6����(F) PEG-MoOx �� X �������䣨XRD��ͼ�ס�(G) PEG-MoOx �ĵ���˳�Ź���EPR�����������(H) PEG-MoOx ���Ż��ռ乹����ʾ����λ��(I) Ce6��PEG-MoOx �� Ce6@PEG-MoOx NPs �ĸ���Ҷ�任������ף�FTIR��
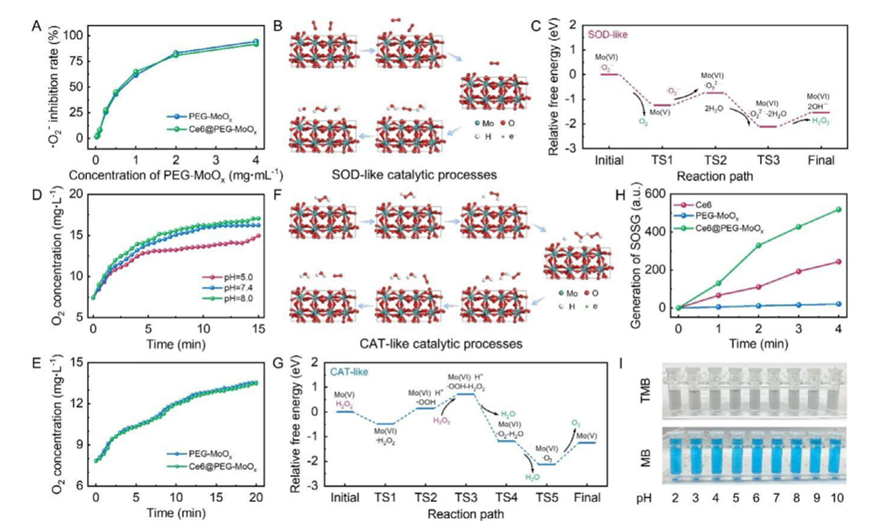
EG-MoOx �Ĵ������� (A) ⋅O2− �����ʣ��� Ce6 ����ǰ��ͨ�� WST-8 �ⶨ�� (B) MoOx �� SOD �����̵ķ���ģ�͡� (C) SOD ������̵� DFT ������������ܡ� (D) ��ͬ pH ������ PEG-MoOx �� O2 ���������� (E) Ce6 ����ǰ�� PEG-MoOx �� O2 ���������� (F) MoOx �� CAT �����̵ķ���ģ�͡� (G) CAT ������̵� DFT ������������ܡ� (H) �� 0.5 mM H2O2 ˮ��Һ�У�ͨ�� 660 nm �������䣬ʹ�õ�̬����������ɫ (SOSG) ̽���� 1O2 ���ɡ� (I) 3,3,5,5-�ļ������� (TMB) ���Ǽ��� (MB) ̽�����ڼ�� PEG-MoOx �ڲ�ͬ pH ֵ�µĻ����� (ROS) ����������
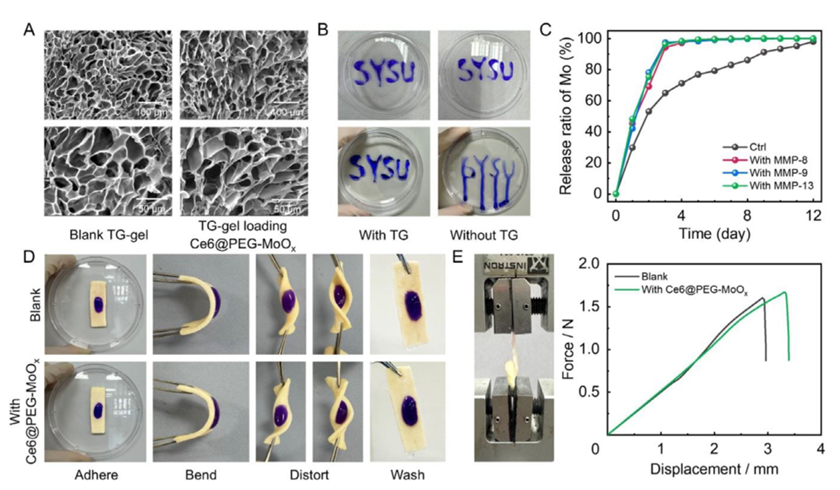
ת�Ȱ�����ø����������TG-������ˮ�����ı�����������Ce6@PEG-MoOx���ݵ������ԡ�(A) TG-����ˮ������ɨ�����������SEM��ͼ��(B) ��37��C�º���TG������������Ϊ��(C) ��Ce6@PEG-MoOx����ˮ����������37��C���˹���Һ�в�ͬʱ���ĵ����ϵ������壨ICP��������(D) TG-����ˮ�����ڸ��ػ���Ce6@PEG-MoOxʱ����Ƥ�ϵ�ճ�����ܡ�(E) ������������֮��ˮ����ճ�ϼ��Ĵ�Ӽ��в��ԡ�
�ܽ�
���ڡ�Advanced Materials�������о�չʾ��һ���������������Ƶ����ܡ�����һ�廯��ˮ����ϵͳ����ɽ��ѧ�о��Ŷӿ�����һ�ָ����������ø��PEG-MoOₓ����������Ce6���Ŀ�ע��ˮ��������ע�䵽�������ܴ������������������コˮ��һ������ճ����������Ӧ���Ի����и�Ũ�ȵĻ��ʽ�������ø��MMPs���������ͷ�����ҩ�
��һϵͳ�ľ���֮�������乹����һ�������ġ��ջ��������������ȣ������ù�������PAI������ʵ�����ܴ���ȵĿ��ӻ�����������⡣����ڽ�����������£��������ø�������������ø��CAT�����ԣ��ֽ�������������������Ч����������֯��ȱ��״̬����������ǿ�˹�����Ce6�Ĺ������Ч�����ɸ�Ч����������������ڵ��������Ĥ�����ɱ��������ø�������೬�������绯ø��SOD�����Ի����������Ļ���������������Ӧ�����ˡ����м�ֵ���ǣ��ͷŵ��������ܼ���PI3K/AKT�ź�ͨ·�ٽ�Ѫ��������ͬʱ�յ�����ϸ�������͵�M2���ͼ��������̼�����Ĥ��ϸ���ijɹǷֻ����Ӷ�Эͬ�ٽ�������Ӳ��֯�������������о��ɹ��ؽ���ϡ����������ʹ���������������һ��������Ӧ�Ͳ���ƽ̨��Ϊ�����ľ��ջ������ṩ�˼����ٴ�ת��DZ�����²��ԡ�
�ο����ף�
DOI: 10.1002/adma.202522859
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ