
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

��������ROS������������������֮��Ķ���ѭ�����ļ�������MI���ĺ��IJ����������ء�Эͬ�ٽ� ROS �������ǿ������������ʵ��������ԭ��̬��������л��˫�ػָ�������Ч�����ļ������Ĺؼ���Ϊ�ˣ����ǿ�����һ�ַ���֥�������塢����������³ʿ������ø��SP���������λ��Ϊ Se0/Fe2+/Fe3+��ͨ����������ø�ij����������ø��SOD�������ԣ������������ӣ���O2�C����ת��Ϊ�������⣨H2O2����ͬʱ�����ϵĹ�������ø��CAT��ģ����Խ�һ���ֽ�����������O2����ͬʱͨ������ǿ���Ӵ���Эͬ���� PINK1/Parkin �鵼�����������ա� �������ø�����Ͻ�ˮ�����У�ͨ��ȩ�����������밷��ܻ�����ø֮��Ķ�̬ϣ�����γ� SP@Gel��ע�䵽�������ļ�������ˮ�����ܹ������ͷ�����ø���� SP@Gel �ڴٽ� ROS ����ͼ����������˷�����ֳ������������Ӷ������ļ�������ԭ����̬�����⣬SP@Gel ��ǿ��������������ͨ������ͨ�� PTEN �յ��ļ��뼤ø 1��PINK1��/Parkin/����ص��� 1 ���� 3�£�LC3B��;�����ظù��̣��ٽ�������ṹ��������л�Ļָ�����Щ����ͨ����л��ѧ�����õ��˽�һ����֤�� SP@Gel ע��鵼�ļ������������ܣ�������С������С��������ά������ǿѪ�����ɣ���������������ܡ���һ���ɵ�����ø-ˮ����ϵͳ�������ļ���������ǰ�����Ʋ��ԣ�ͨ������Ӧ�����������������Ƶ�˫�ص���ʵ��Эͬ���ơ�
 ���о�����Ϊ��Biomimetic Selenium-Encrusted Prussian Blue Nanozyme for Myocardial Infarction by Coordinated Enhancement of Mitophagy and Reactive Oxygen Species Scavenging��������ACS Nano�ϡ�
���о�����Ϊ��Biomimetic Selenium-Encrusted Prussian Blue Nanozyme for Myocardial Infarction by Coordinated Enhancement of Mitophagy and Reactive Oxygen Species Scavenging��������ACS Nano�ϡ�
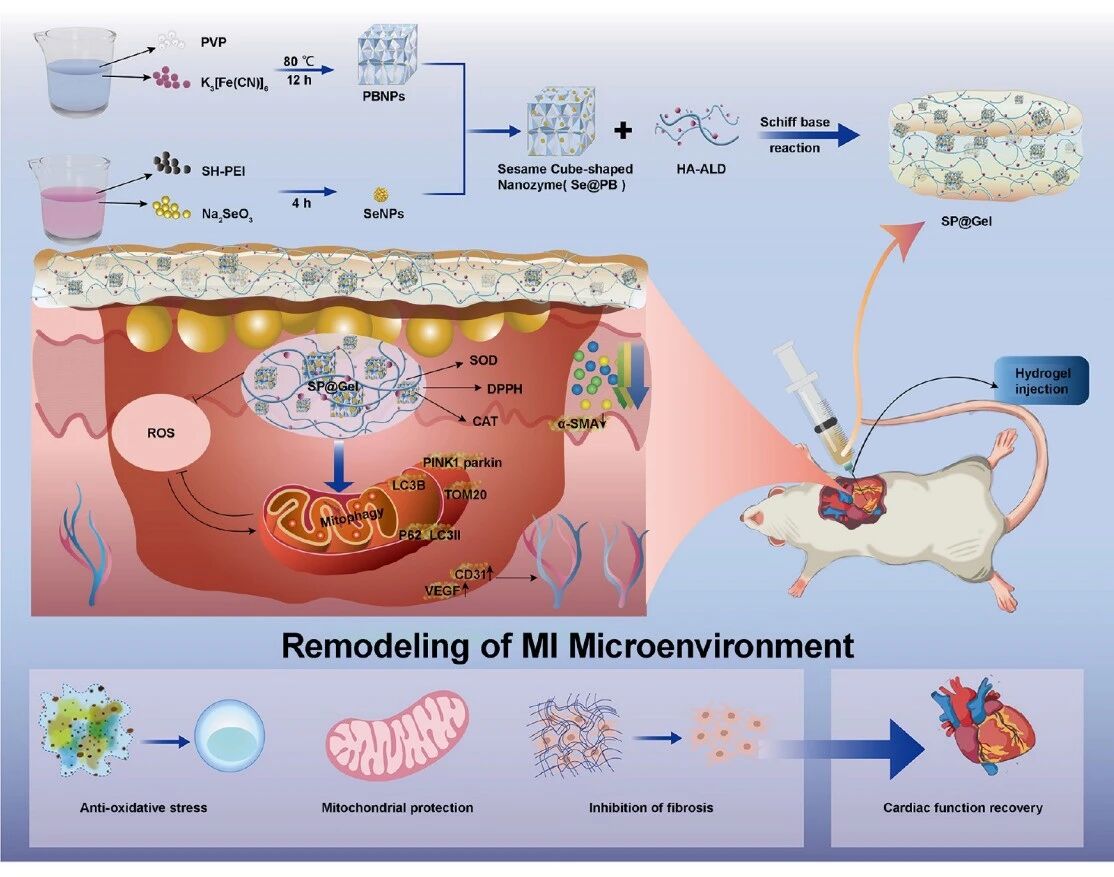
������������³ʿ������ø����ˮ����ͨ��Эͬ��ǿ���������ɺͻ�������������ļ���������
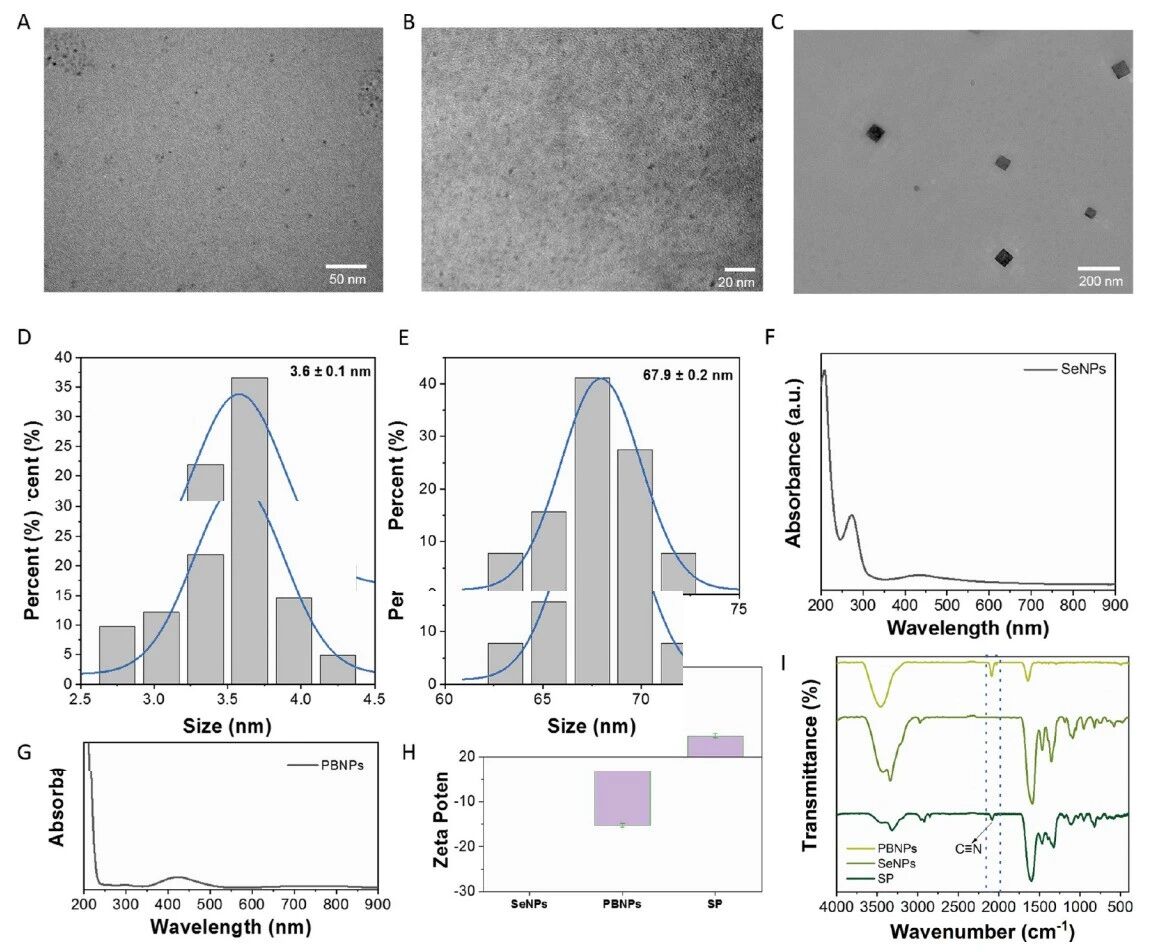
�������ĺϳ��������A�������������������������ͼ�������ߣ�50���ף�B���������������ĸ߷ֱ������������ͼ�������ߣ�20���ף���C�������������������������������ͼ�������ߣ�200���ף�D�����������ijߴ�ֲ�ֱ��ͼ��E���������������ijߴ�ֲ�ֱ��ͼ��F������-�ɼ�����
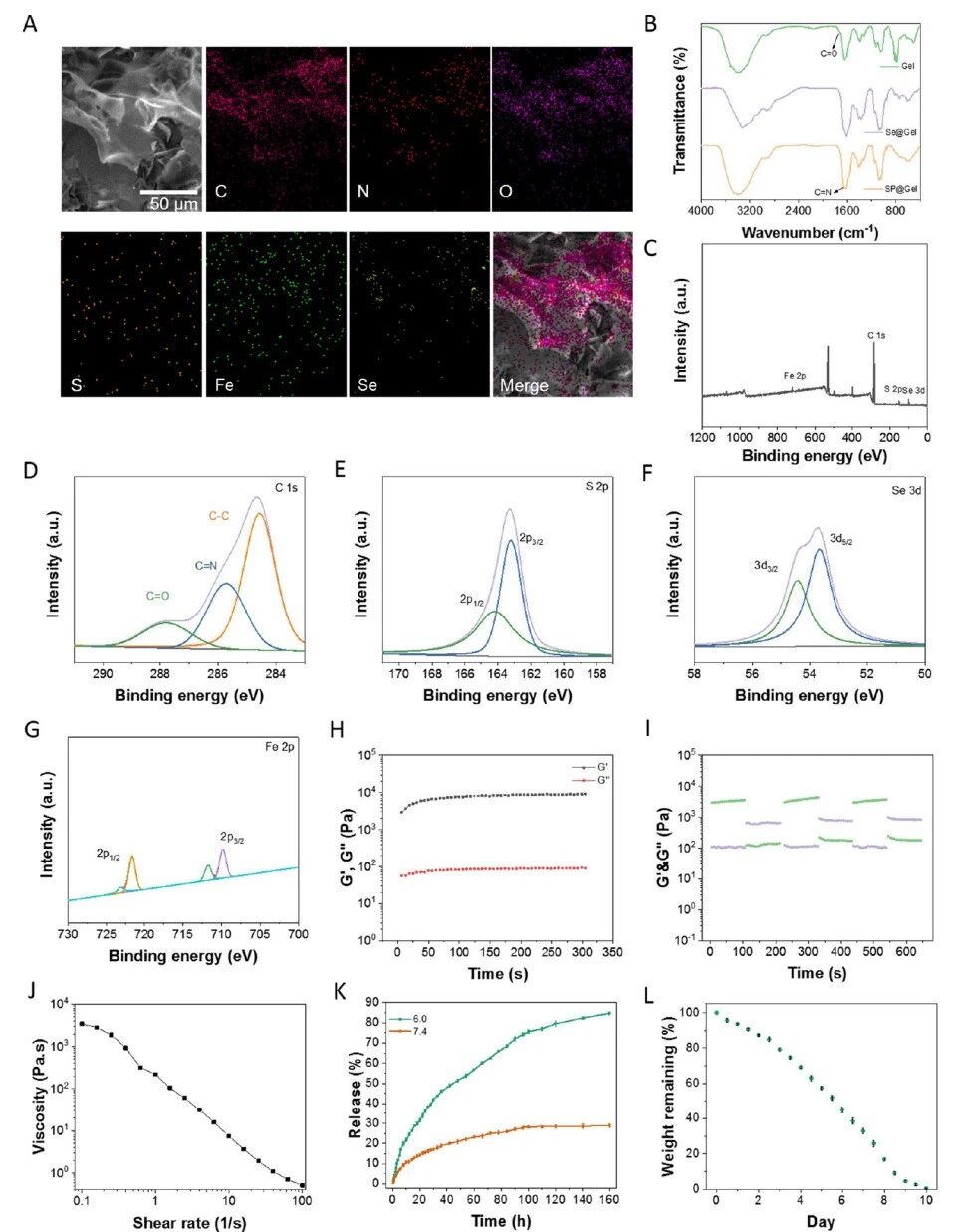
�ܽ�
�Ĺ�����ӭ����˼·��һ���ܡ���ɨ������������ķ�������øˮ�������Ĺ����ļ�ϸ�������롰�������������롰���������ˡ��Ķ���ѭ��������������������ͳ�������ָܻ�Ѫ����ȴ����ͬʱ���������������⡣���գ�һ����ڡ�ACS Nano�����о�������һ��ȫ�µķ������ԣ��о��Ŷӽ���Ԫ������Ƕ����³ʿ����������������һ�����ơ�֥������Ķ�ø��������ø�����СС�Ŀ����ɲ������������/������λ��������������绯øһ������к��ij��������ӣ��������������øһ��������ת��Ϊ�������൱�ڸ�ϸ���䱸��һ��Ч�ġ��ⶾϵͳ����
����Ȥ���ǣ��������뻹�����˲��ϡ����ܡ����ԡ�����ֻ��������Ĥ��λ�쳣ʱ������PINK1/Parkinͨ·���������������������������о��Ŷӽ���������ø��װ����ע���ˮ������ע�䵽�Ĺ������ˮ�����ܳ����ͷ�����ø��ʵ������ʾ�������Ʒ���������������ļ��ڵĻ�����ˮƽ����ͨ���ٽ����������ɻָ���������л�����Ĺ�����ģ���У��������Ƶ��ļ���ά�����������С������Ѫ���������࣬����ı�Ѫ����Ҳ�õ���ʵ���Ը��ơ���һ��ƽ��������������������������������Ժ϶�Ϊһ��Ϊ�Ĺ����������ṩ��ȫ�µ����Ʒ�ʽ��
�ο���Ϣ��
DOI: 10.1021/acsnano.5c17071
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ