
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

��������������ԭʧ���������ڹǹؽ��ף�OA����չ�����Źؼ����á����ܿ���������ø��������DZ��������Ƹ�Ч�Ұ��������������ϵͳ�Ծ���ս�ԡ����ǿ�����һ�ֶ�ά������ʯīϩ����������NGM����װ�طǶԳ��Ҹ߶ȱ�¶������ԭ�ӣ���Я���������ǵ� WYRGRL �ĺ� siRNA��siMMP13�����γ���ø��si-FeSA/NGM-W������Ϊ���������Ƽ��Ի���ǹؽ��ס�ͨ��������κ�пȥ������ Zn-ZIF ȥ���ʳɾ�������ȱ�ݺͲ㼶�ṹ�ij�����ά�㼶��� NGM �ṹ�����Ǵ�����һ������ê���ǶԳ��Ҹ߶ȱ�¶������ԭ�ӵ�֧�ܡ��ḻ�� Fe�\N 4 �\Cl ��λ����λ������Ӧ���ȱ�ݣ��ٽ�����ת�ƣ���ǿ���ɻ����������ͷ�Ӧ���ϣ��Ӷ���ǿ��ø��SOD/CAT/GPx�����ԡ���ʹ���ܻ��� si-FeSA/NGM-W �ܹ��������ǣ�ͨ���µ� MMP13���ϵ� GPX4���ָ������幦�ܺ͵�����֢������������������ʵ�ְ���ǹؽ������ơ��ӻ����Ͻ����ù����漰���� IL-17 ͨ·����ǿ�����Ĵ�л������������һ�ְ�������øƽ̨������ͨ�����������ƾ�ȷ���� OA��

���о�����Ϊ��Engineering Asymmetric and Highly Exposed Fe Single-Atom Nanozymes for siMMP13 Delivery and Ferroptosis Inhibition in Osteoarthritis Therapy��������Advanced Materials�ϡ�
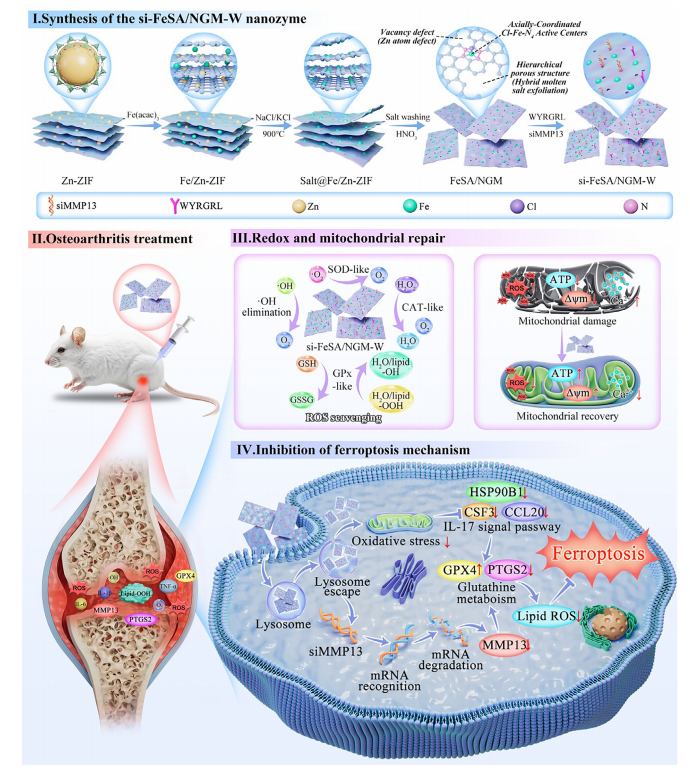
si-FeSA/ NGM -W�ϳ�ʾ��ͼ������SOD��CAT��GPx�����������ROS����ԭ��
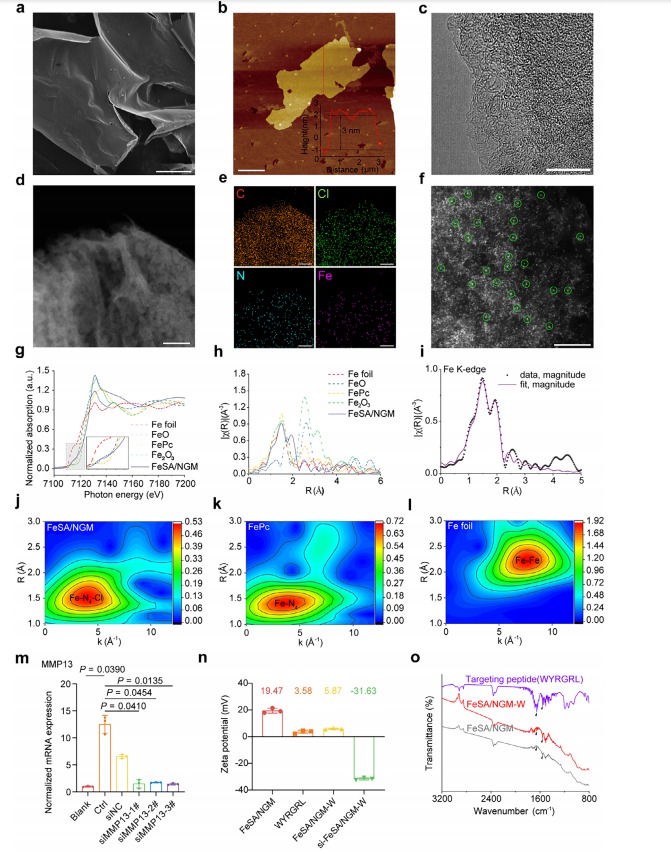
(b)ԭ��������(AFM)��ò����Ӧ�߶ȷֲ�ͼ����ͼ���������ߣ�200���ס�(c)���������(TEM)ͼ�����ߣ�200���ס�(d��e)FeSA/ NGM SAzyme������ɫɢ��(EDS)ӳ��ͼ�����ߣ�100���ס�(f)���У���߽ǶȻ��ΰ���ɨ�����������(AC- HAADF -STEM)ͼ����ʾԭ�ӳ߶Ƚṹ
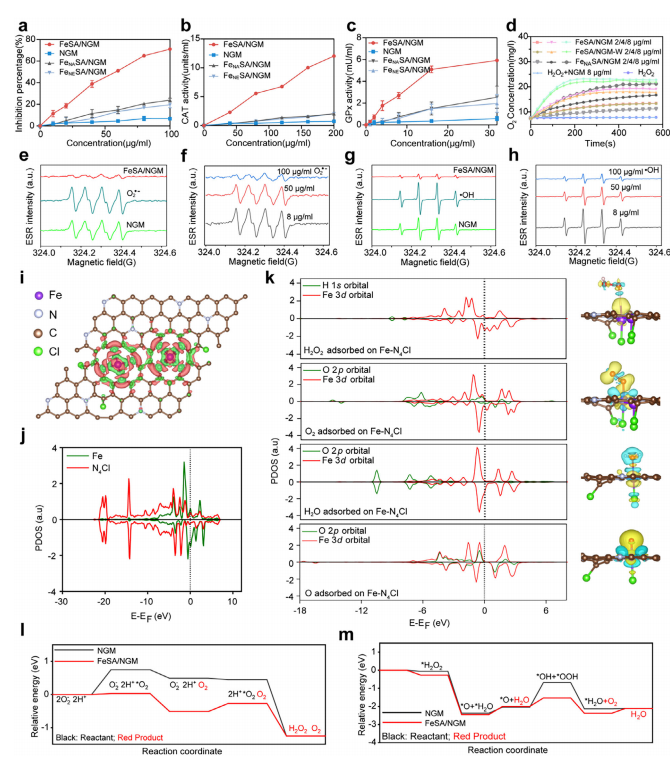
FeSA/ NGM ����ø��ø��������ӽṹ������(a-c) FeSA/ NGM ��FeNASA/ NGM ����ø��(a)���������绯ø(SOD)��(b)��������ø(CAT)��(c)�����Ĺ�������ø(GPx)���Ե�Ũ��������ģ�⡣(d) ͨ����ͬŨ��������ø�����O2��������������������ֽ�Ч�ʡ�(e-h) ������������(ESR)����ʾFeSA/ NGM �Ļ��������������(e��f) ��ͬŨ���³������ɻ�(O2∙−)��������(g��h) �������ɻ�(∙OH)��������(i��j) ���ӽṹ������(i) ��ֵ���ܶȷֲ���(j) FeSA/ NGM ��ͶӰ̬�ܶ�(PDOS)����ɫ/��ɫ�����ʾ���ӻ���/�ľ���(k) FeSA/ NGM �Ϲؼ��м���(�������⡢O2��ˮ��O)������������ PDOS ������(l��m) ģ��SOD/CAT���Ե�FeSA/ NGM �Ϲ������ԭ·���������ܱȽ������� NGM �����顣����ֵ�ѹ�һ������ʼ��Ӧ��״̬(0 eV)�������Ծ�ֵ�������ʾ(n=3)��
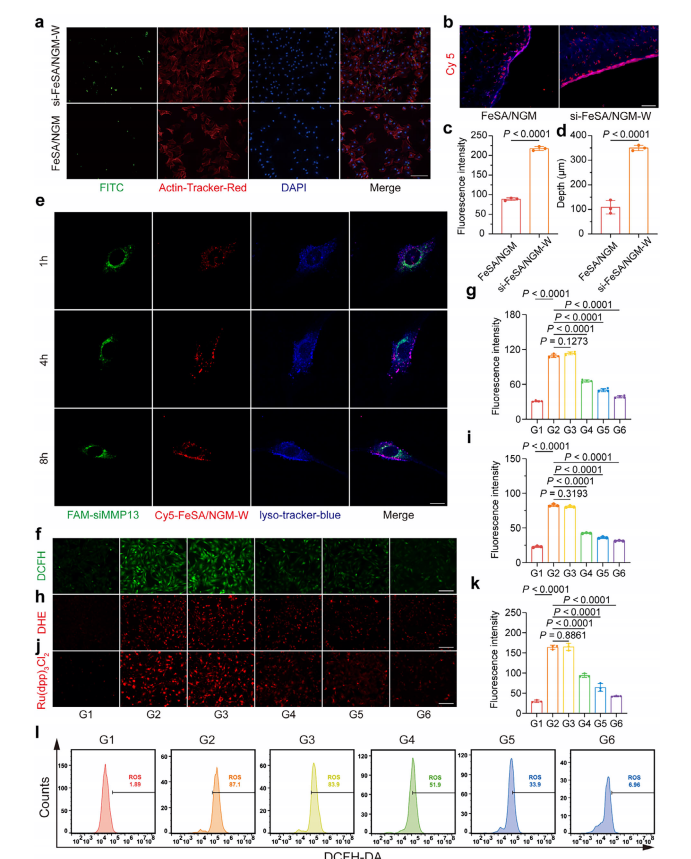
si-FeSA/ NGM -W����ø������ϸ��ģ���еĶ�ģ̬���ܱ�����(a��c)����12Сʱ�� FITC ��ǵ�FeSA/ NGM ��si-FeSA/ NGM -W��ϸ����ȡ����ѧ��(a)�����Թ��۽�����ͼ��(c)ӫ��ǿ��ͨ��ImageJ�������������������ߣ�100 µm ��(b��d)Cy5�������ø������ؽ������еİ���Ч�ʡ�(b)ӫ��ֲ���(d)ӫ���������������ߣ�1000 µm ��
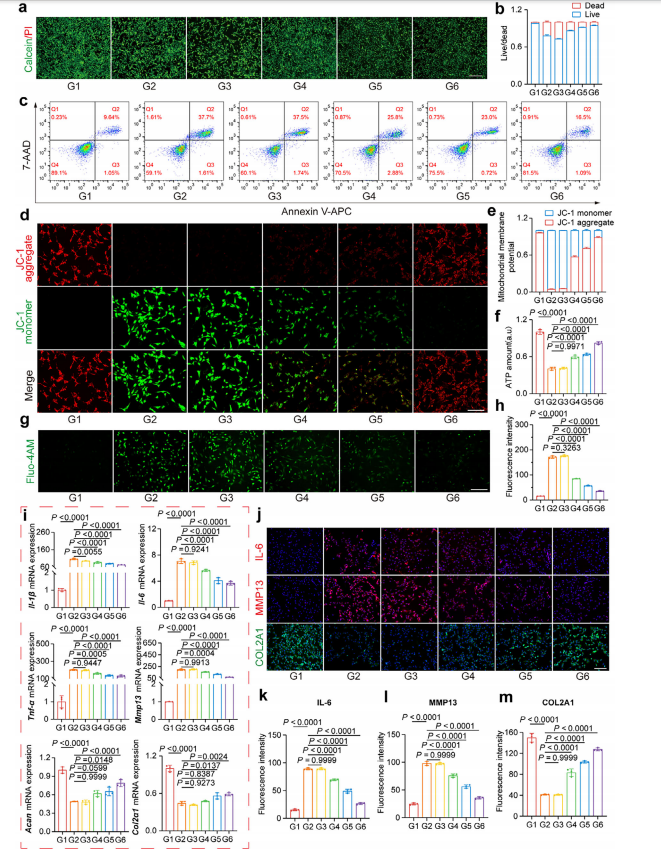
SAzymesͨ�������������ROS����������ϸ�����ڵ�������֢�Ļ����о���(a)�ƻ�����AM����ɫ����ϸ������⻯��ण�PI����ɫ����ϸ����Ⱦɫ������ϸ�������Թ��۽�����ɨ��������CLSM��ͼ�����ߣ�500 µm ��(b)��/��ϸ�����ʵĶ���ӫ�������(c)ͨ��AnnexinV-APC/7- AAD Ⱦɫ����ʽϸ��������������(d)ͨ�� JC -1Ⱦɫ������������Ĥ��λ CLSM ͼ�ۼ��壺��ɫ�����壺��ɫ����
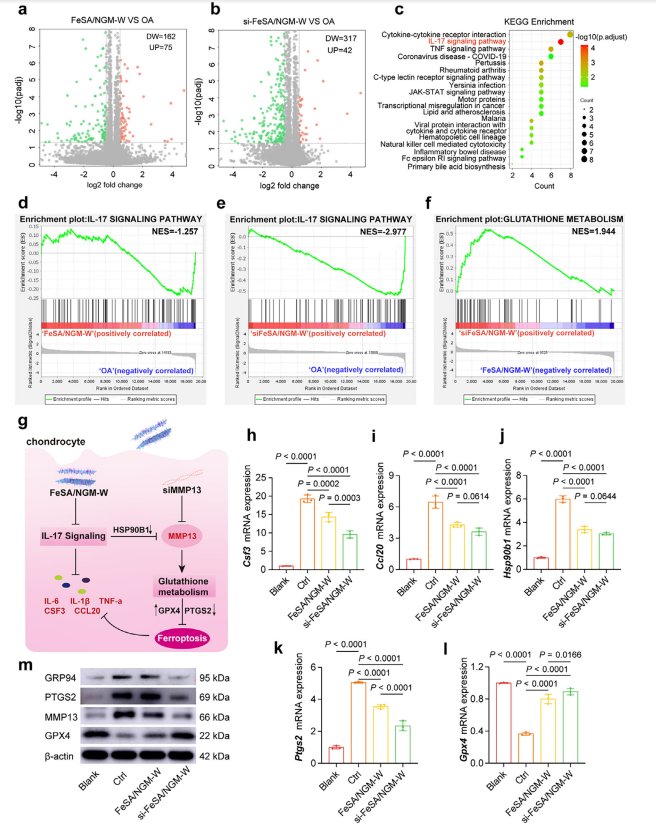
����SAzymes����ǹؽ���DZ������ѧ���Ƶ��о���(a)��ɽͼ��ʾFeSA/ NGM -W����OA��mRNA����仯��(b)��ɽͼ��ʾsi-FeSA/ NGM -W����OA��mRNA����仯��(c)�������� KEGG ���������(d��e)IL-17ͨ· GSEA ͼ��(f)�����Ĵ�л GSEA ͼ��(g)FeSA/ NGM -W��si-FeSA/ NGM -W����OA��DZ�ڷ��ӻ��ơ�(h-j)IL-17ͨ·��ػ����qPCR������(k��l)��������ػ����qPCR���������(m)�Լ�������Ϊ�ڲε�����ϸ����IL-17ͨ·����������ص���Western blot��⡣�����Ծ�ֵ�������ʾ(n=3)��Pֵͨ�������ط���������������Ǻű�ǡ�
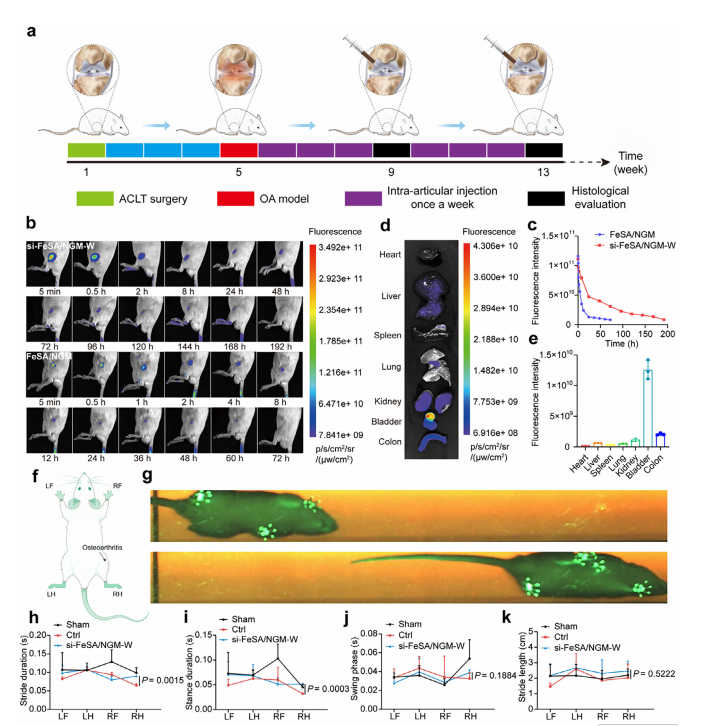
SAzyme������OAģ�͵���������ֲ����ؽ���������̬������(a) FeSA/ NGM ����ø�鵼��OA���ڻ���ʾ��ͼ��(b) ϥ�ؽ���ע���OA�յ�����ϥ�ؽ���Cy5��ǵ�FeSA/ NGM���ϣ���Cy5��ǵ�siFeSA/ NGM -W���£���ʱ��ӫ�����(c) ϥ�ؽ�ӫ��ǿ�ȵĶ���������(d) FeSA/ NGM -Wϥ�ؽ���ע��24Сʱ����Ҫ���٣����ࡢ���ࡢƢ�ࡢ�κ����ࣩ������ӫ�����(e) ����ӫ���źŶ���������(f��g) ��̬����ʾ��ͼ��Ϊ��¼��̬����OA��������ѹ����Ӧ����У���¼��ǰצ��LF�������צ��LH������ǰצ��RF�����Һ�צ��RH�����˶���(h�Ck) �������鲽̬�����Ƚϣ�����(h)��֧����(i)���ڶ���(j)�Ͳ���(k)�������Ծ�ֵ�������ʾ��n=3����Pֵͨ�������ط�����������������Ǻű�ע��
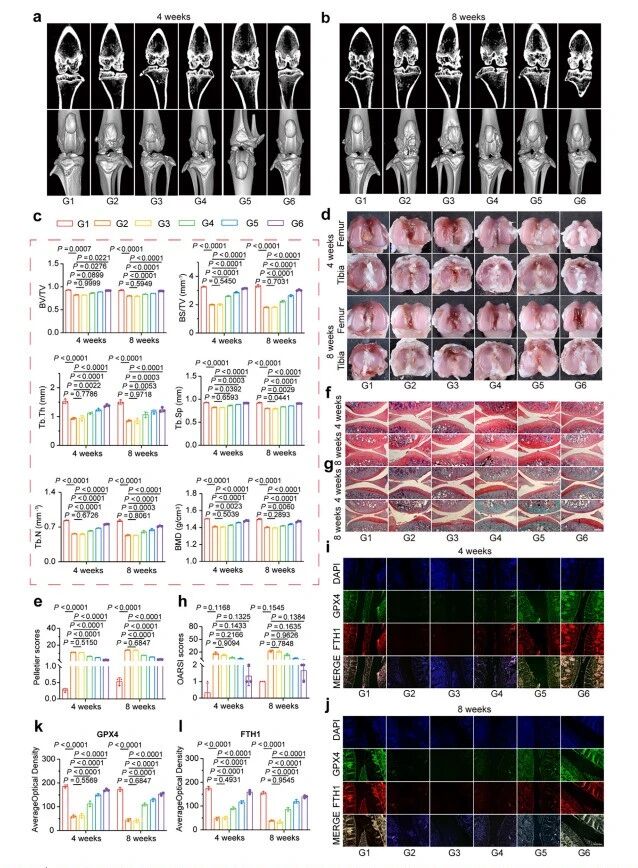
OA�Ʒ�������ЧӦ��(a��b) CTͼ��չʾ�����ƺ�4�ܺ�8��ʱ��Ӧ���Ƶ�Ч����ͼ���Զ�ά��ʽչʾ�ڶ�������ά��ʽչʾ�ڵײ���(c) ͨ��CT�����������������ֹ�С�����������ڹ������Ķ����������������������������BV/TV�����DZ����ܶȣ�BS/BV����С����������Tb.N����С���ǽṹ��ȣ�Tb.Th����
�ܽ�
�ǹؽ��Ľ�չ������ϸ����������������ء����������ѻ��������ĺĽߡ�GPX4ʧ����յ������������ͻ��ʽ��⡣����ҽ�ƴ�ѧ���п�Ժ�����������Ŷ��ڡ�Advanced Materials�������о��������û�����ΰ�����ԣ���Zn-ZIFǰ��ת��Ϊ������ά������ʯīϩ����������������ê�����Գ���λ��Fe-N4-Cl��ԭ��λ�㣬��ż�����ǰ�����WYGRGL��MMP13��siRNA��������һ����Ϊsi-FeSA/NGM-W�Ķ������ø��
����ṹ��Ƶľ���֮�����ڣ���ά���������������ԭ�Ӹ߶ȱ�¶��Fe-N4-Cl�IJ��Գ���λ�յ�����Ӧ���ȱ�ݸ��������ٵ���ת�ƣ����ͷ�Ӧ���ݡ�DFT������ʾ��Fe��d���������ƣ������м�����ӻ���ǿ��ʹ��SOD��CAT��GPx����ø��Эͬ�����������ܽ�����������ת���ɹ������⣬���ܰѹ�������ֽ��ˮ����������ǻ����ɻ����൱�ڸ�����ϸ��װ��һ�������Ŀ�������ˮ�ߡ�����ʵ���8��/������si-FeSA/NGM-W��H₂O₂�յ��Ļ��������64.5%��������Ĥ��λ�ָ�91.7%��IL-1�º�MMP13�ı��ﱻ������ס��GPX4����������ת¼������ʾ���ⱳ����IL-17ͨ·�����ơ������Ĵ�л�����
�ο���Ϣ��
DOI: 10.1002/adma.202520951
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ