
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

�ͺ��������˵ķ�չ�������������ҽѧӦ���ж����ܶ�ܻ���������������ͻ�����ϵͳ����ʵ����ЩӦ����������ԡ����ǽ����˾��п������˶�����ǿ���オ���ԡ������ڳ���Աȶ��Լ���Ч����ʹ�������λ��ø���ݻ����ˡ���Щ�ͻ����˲��þ�����ø�������Ȼ�����壬�ֽ���������õ�����ʵ�������ƽ������ڲ�������Ϊ�����֯����͵�������������Աȼ�����������������ʹ���������Ĵſ��˶���Ϊ���ܣ���������ܻ��ٽ���������������ݶ��ƶ�������������ǰ��������λ���۽������ᴥ�������˿���̮�����ͷ��ݵ����Կ�ʴ��������е������ǿ������Ч�غɵĴ��������о���֤����Щ�����˵��������������Ч������ʾ����ǿ�Ŀ�����Ч������һ����ݻ�����ƽ̨��DZ���ı�ҽ�Ƹ�Ԥ�;����ơ�

���о�����Ϊ��Enzymatic microbubble robots��������Nature Nanotechnology�ϡ�
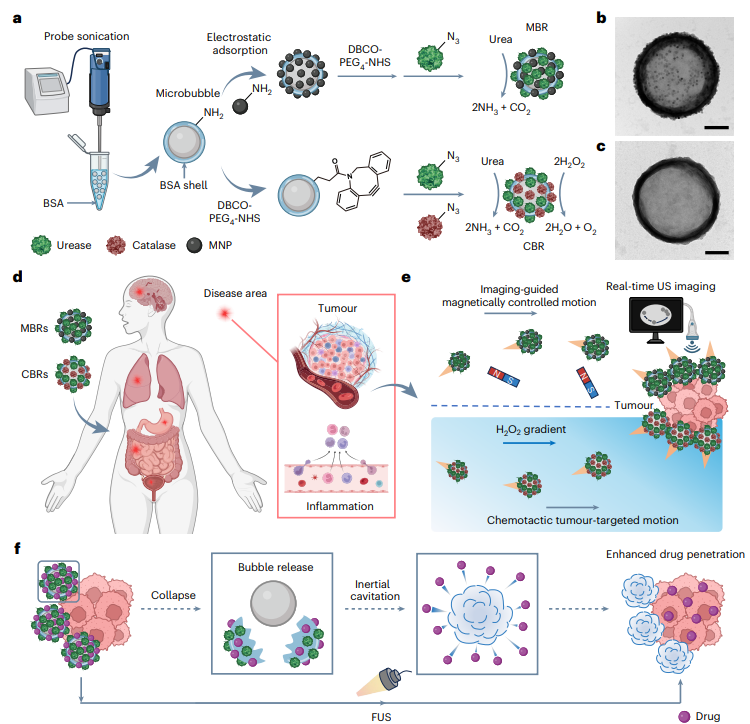
�����オ���ݻ����˵ĸ��������Ǿ߱���Ч�����ƽ����߳���Աȶȡ�������λ��������ǿ��֯��������a��ø�ݻ������Ʊ�����ʾ��ͼ��ʹ��̽�볬�����Ʊ��˾���BSA�ǵ��ݣ�MBRͨ������������MNP���������ϣ�Ȼ��ͨ�������ѧ�̶�����ø���Ʊ���Ϊ�˴���CBR��ͨ�������ѧ������ø��������ø����ݱ��档b,c��MBR��b����CBR��c����TEMͼ�����ߣ�200 nm��d,e��MBR��CBR���ü�����λʾ��ͼ��d����������ɿ��ƽ���������MBR�ij������ŵ��˶���CBR������������������˶���e����f��FUS�յ�ҩ�����ݻ�����̮���������ݿջ�ʾ��ͼ��ּ����ǿҩ���������֯������ͼa��d�Cf��BioRender.com������
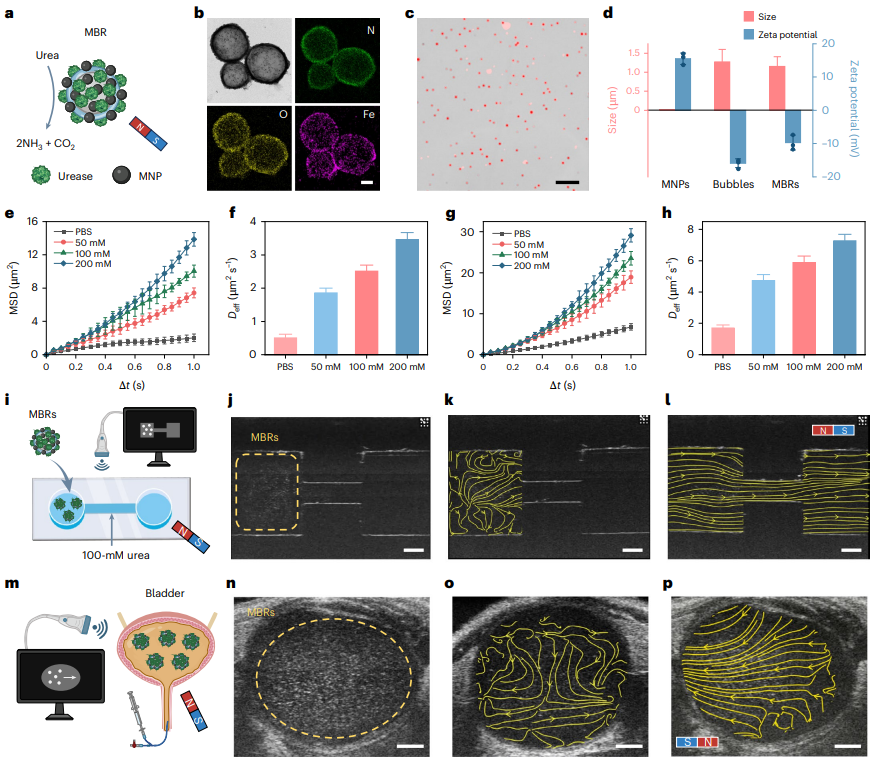
MBRs�ı�����a����������ø��MNPs��MBRʾ��ͼ��b��TEM��EDSӳ��ͼ����ʾMBRs�е�(N)����(O)����(Fe)�ķֲ��������ߣ�200 nm��c��������ӫ��ͼ�������ʾ��Cy3�����ø���ε�MBRs�������ߣ�10 ��m��d��MNPs�������ݺ�MBRs�ijߴ缰�Ƶ�λ�������������ʾ50��MBRs�ľ�ֵ����Լ��ߴ�ͦƵ�λ�����β�����e,f��MBRs��������Һ�еľ���λ��(MSD) (e)����Ч��ɢϵ��(Deff) (f)��g,h��MBRs��������Һ���ܴſ��µ�MSD (g)��Deff (h)��e�Ch�е��������ʾ15��MBRs�ľ�ֵ���i,j���������к�100 mM���ص�MBRs�������������ſ��ƽ�ʾ��ͼ(i)����Ӧ�ij���ͼ��(j)�������ߣ�1 mm��k,l��PIV�����õ�������ģʽ����ͼ����ʾ��������MBRs����(k)����(l)��Ӵų��µ��˶��������ߣ�1 mm��m,n��С�������MBRs�ſ��ƽ���ʾ��ͼ(m)��ʵʱ�������������µij���ͼ��(n)�������ߣ�1 mm��o,p��PIV�����õ�������ģʽ����ͼ����ʾС�������MBRs����(o)����(p)�ſ��µ��˶���j�Cl��n�Cp�ij���Ƶ�ʣ�50 MHz�������ߣ�1 mm
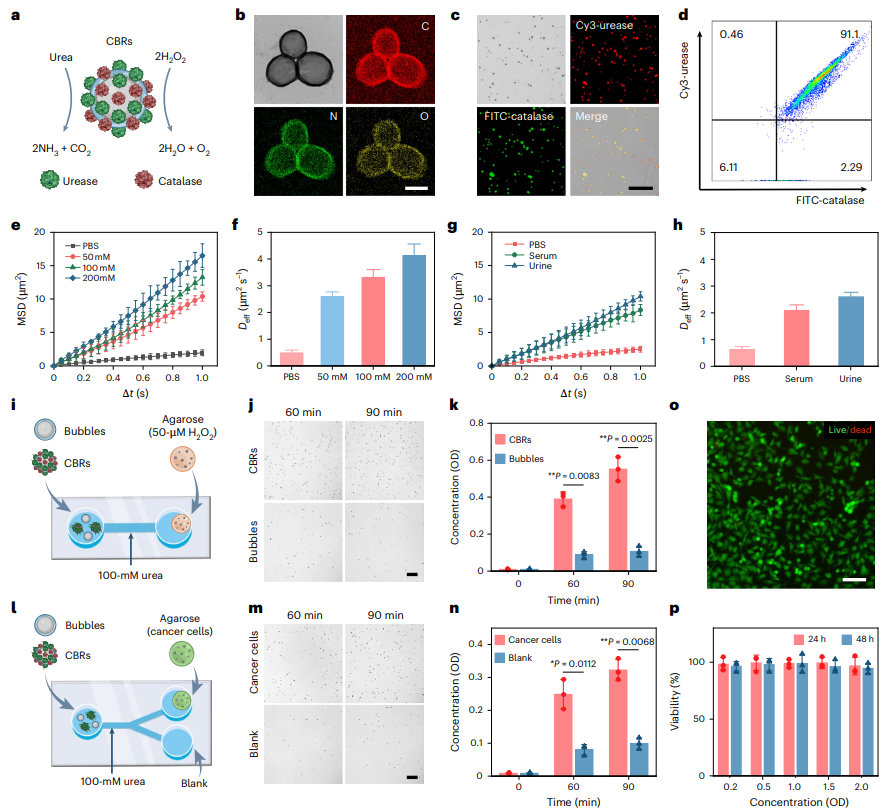
CBR�ı����� a����������ø��������ø���ε�CBRʾ��ͼ�� b�������������TEM�������ף�EDS��ӳ��ͼ����ʾCBR��̼��C��������N��������O��Ԫ�صķֲ��������ߣ�500 nm�� c������Cy3��ǵ�����ø��FITC��ǵĹ�������ø���ε�CBR������ӫ��ͼ�����ߣ�20 ��m�� d��ͨ���������ѧ������ø��CBR������Ч�ʵ���ʽϸ������ e,f��CBR��������Һ�еľ���λ�ƣ�MSD, e������Ч��ɢϵ����Deff, f���� g,h��CBR��PBS����50 mM���ص�FBS��С����Һ�е�MSD��g����Deff��h���� e�Ch�е�����߱�ʾ15��CBR��ƽ��ֵ��� i������CBR�������һ�ѧ�����˶���װ��ʾ��ͼ���ҲഢҺ�����ɺ�50 ��M H2O2����֬�������γ�H2O2�ݶȡ� j,k������60��90���Ӻ��ҲഢҺ���еĴ����Թ�ѧͼ��j����CBR�����Ķ�����k����OD�����ܶ�OD500��1 OD �� 10^8 ����/ml�������ߣ�20 ��m�� l������CBR��Y�������һ�ѧ�����˶���װ��ʾ��ͼ���ҲഢҺ��֮һ�ɺ��ѽ�T24���װ�ϸ������֬�������γ�H2O2�ݶȡ� m,n������60��90���Ӻ������ҲഢҺ�۵Ĵ����Թ�ѧͼ��m����CBR����������n���������ߣ�20 ��m�� o,p����CBR������2 OD 48Сʱ��T24ϸ���Ļ��ɫ��/������ɫ��������ͼ��o�����Բ�ͬŨ��CBR����24��48Сʱ���ϸ������������p���������ߣ�100 ��m�� k��n��p�е�����߱�ʾ���β�����ƽ��ֵ��� k��n�е�ͳ�Ʒ���ʹ�����˫βt���顣*P < 0.05��**P < 0.01
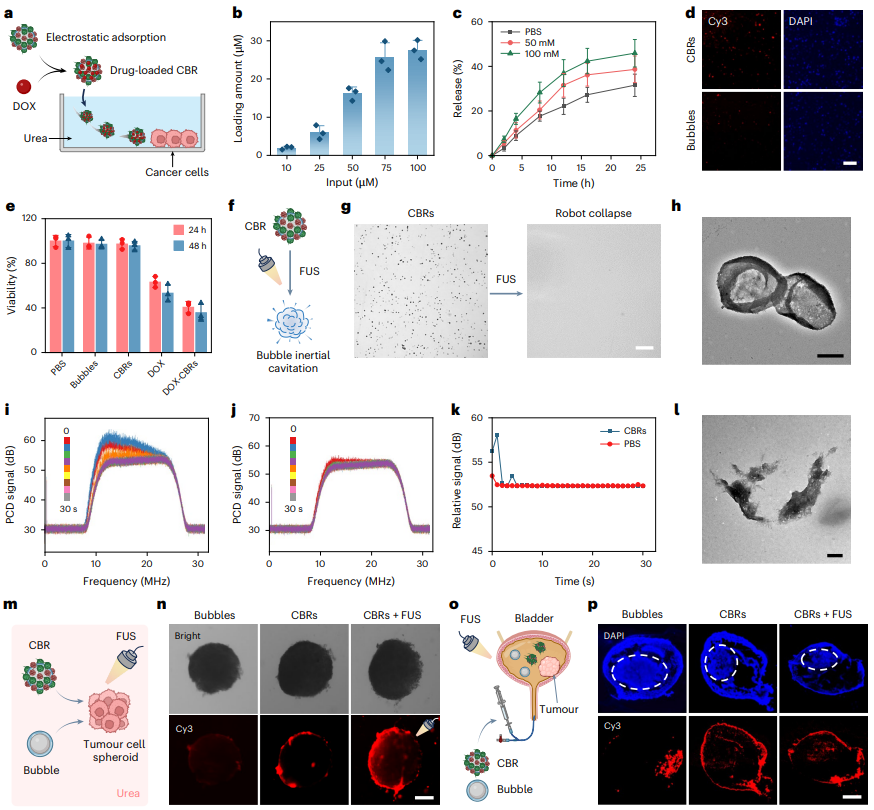
�ݻ�������ҩ�︺�ء�������Ϻʹ������������a�������ҩ����͵Ķ�����Ǹ���CBRs��DOX-CBRs��ʾ��ͼ��b����ͬҩ����������CBRs��4Сʱ������ĸ�������c��DOX-CBRs��������Һ�е�ҩ���ͷ����ߡ�d��ӫ��ͼ����ʾCy3��ǵ�CBRs��������100 mM��������T24���װ�ϸ�����2Сʱ�������������ߣ�100 ��m��e��T24��ϸ����100 mM�����д������ݡ�CBRs������DOX��DOX-CBRs 2Сʱ����ϴ����һ������22��46Сʱ��ϸ��������b��c��e�е�����ߴ�������ʵ��ľ�ֵ���f,g��ʾ��ͼ��f��������ͼ��g����ʾCBR�ڽ�������FUS���̼��µ���������������ߣ�20 ��m��h��TEMͼ����ʾFUS���������ѵ�CBR���塣�����ߣ�500 nm��i�Ck�������峬���̼���CBRs (i) ��PBS (j) �Ļز�Ƶ�ף��ɼ�ʱ��Ϊÿ��һ�Σ���30�룬�Լ���Ӧ��ƽ�������ź� (k)��l��TEMͼ����ʾ����CBR����0.25%�ȵ���ø����12Сʱ��Ľ�������������ߣ�500 nm��m,n��ʾ��ͼ��m����ӫ��ͼ��n����ʾCy3��ǵ����ݡ�CBRs��������¶5��FUS��CBRs��100 mM��������T24ϸ�����Ϻʹ�2Сʱ�������������ߣ�100 ��m��o,p��ʾ��ͼ��o����ӫ��ͼ��p����ʾ�����������У�Cy3��ǵ����ݻ�CBRs��2Сʱ������ע���ķֲ������CBRs����2Сʱ��ʩ��FUS������������DAPI����ɫ��Ⱦɫ����ɫ���߱������λ�á������ߣ�1 mm��
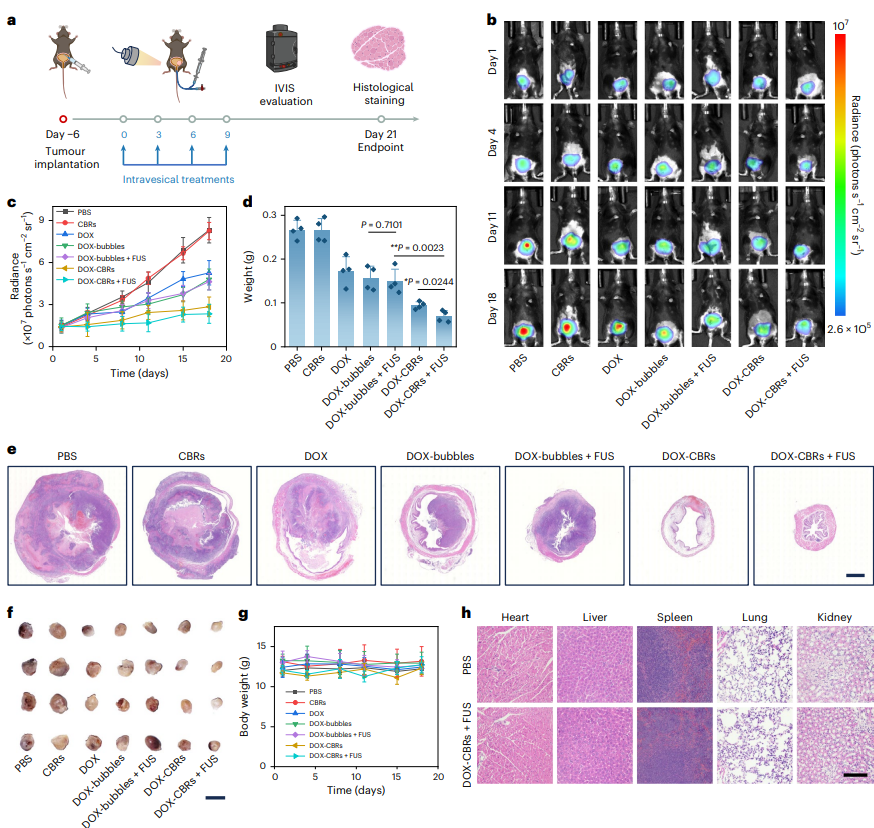
����ԭλ��������ģ�����������ݻ����˿�����Ч����a, ʾ��ͼ˵������Я��ԭλ����������С��ģ�ͼ��������̡�b,c, ����С����עPBS��CBRs������DOX����DOX���ݡ���¶��FUS 2Сʱ���DOX�ݡ�DOX-CBRs��DOX-CBRs + FUS��Ĵ�������������ӫ��ͼ��b������������ӫ��ǿ�ȶ��������c����d�Cf, ���ƽ�������21�죩ʱ����С���г���������(d)��H&EȾɫ(e)��ͼ��(f)�������ߣ�1.5 mm (e)��1 cm (f)��g, С�������������ڼ�����ء�c��d��g�е��������ʾ������ֻС��ľ�ֵ���d�е�ͳ�Ʒ������õ����ط��������*P < 0.05��**P < 0.01��h, ���ƺ�����С���г�����Ҫ���٣����ࡢ���ࡢƢ�ࡢ�κ����ࣩH&EȾɫ��������ΪPBS��DOX-CBRs + FUS�������ߣ�100 ��m�����a��BioRender.com������IVIS�����ڳ���ϵͳ��
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ