
��ѯ���ߣ�
17715390137
18101240246
18914047343
�ʼ���mxenes@163.com
ɨ���ע�����������ںţ�
������Fronrier
��ע�������½���ϵ���ǣ�
������ҵ�š�
רҵ��������

���ڷβ���Ѫ�����������������������ת���ڰ�֢�����й�����ս����ͳ��Ƥ������ͨ������ת�Ʋ�λ�����ֲ����߷�Ӧ��Ϊ�ˣ��������̻��˾��б��� ClyA-OVA257-264 ��ϸ��Ĥ���ݣ�������һ�ֿ�������������� BMVax��ϸ��Ĥ�����磩���������ߴ̼�Ĥ���ĵ�������ѧʵ���˸�Ч�Ŀ�ԭ�����͡�BMVax ȷ���˿�ԭ������֣��ȿ�ԭ+BMV ������� 2.2 �������ƶ���ǿ���Ŀ�ԭ������ T ϸ����ֳ������ἤ������֧�����ܰͽ��ǿ�����߷�Ӧ����ǿ��ֳ���� B ϸ������5.8 ���������ݸ��� T ϸ������4.9 �����ͳ�����ͻ״ϸ������2.5 ������ʵ�� 83.3%�ķ�ת��Ԥ���ʡ��� B16-OVA ��ת��ģ���У�����ʽ BMVax ���������Ʒ�������Ƥ�¸�ҩ������ʹ�ܰͽ��������� B ϸ���������������ݸ��� T ϸ���������� 2.9 ��������֯�п�ԭ������ T ϸ����������Ƥ�����߶�� 2.9 ������������ T ϸ�����ֳ���ǿ��ϸ�����Ժ���ֳ������ǿ���������Ƥ�����ߵ��������ơ���Щ�������� BMVax ��Ϊһ�������Ͱ�֢�����DZ�����ܹ�����ǿ�ҵ����߷�Ӧ����Ч�Կ��β�ת���Զ���������

���о�����Ϊ��Inhalable Nanovaccine Based on Bioengineered Bacteria-Derived Membrane Vesicles Against Lung Metastasis��������Advanced Materials�ϡ�
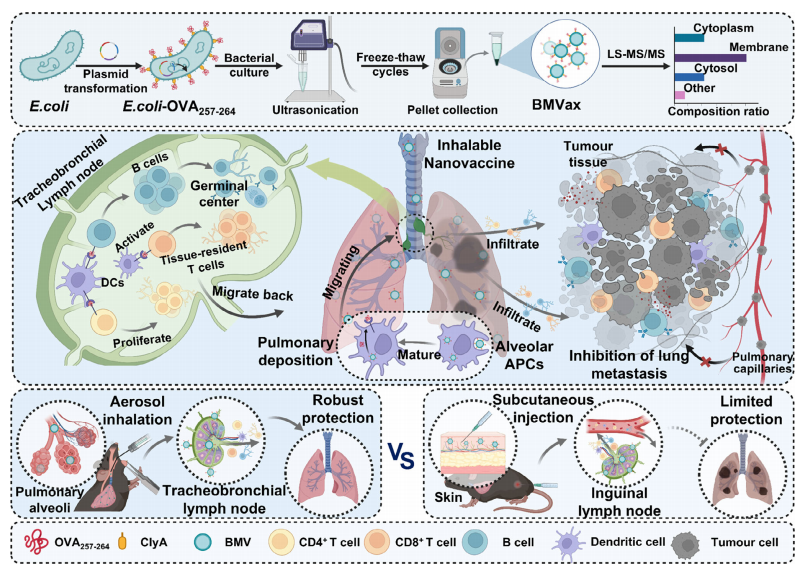
��������������Կ���ת�Ƶ�ʾ��ͼ���������������﹤��ϸ��������Ĥ������ͨ�����̣�ģ�Ϳ�ԭOVA257-264��ϸ���б��ﲢ��������Ĥ�ϡ�������Щ���̻�ϸ������ȡϸ��Ĥ���ݣ������������������磨BMVax�������β�ֱ�ӵ��ͺ�BMVax�������еĿ�ԭ�ʵ�ϸ����APCs����Ч�ڻ������Ǩ��������֧�����ܰͽᣨTBLNs����������ԭ������Tϸ����Bϸ����Ӧ���ù��̴�ǿ�ҵ��������ģ�GC����Ӧ���Ӷ���ǿ�Ĥ���ߡ���Ƥ�½�����ȣ�BMVax�ķβ�ֱ�ӵ����ܸ���Ч��ļ����ԭ������Tϸ�����β������ٽ���֯פ������Tϸ�����γɣ�ȷ�������������ӡ���ˣ�BMVax�ķβ�ֱ�ӵ��ͶԷ�ת���ṩ������������������Ϊ��Ч�����������DZ����
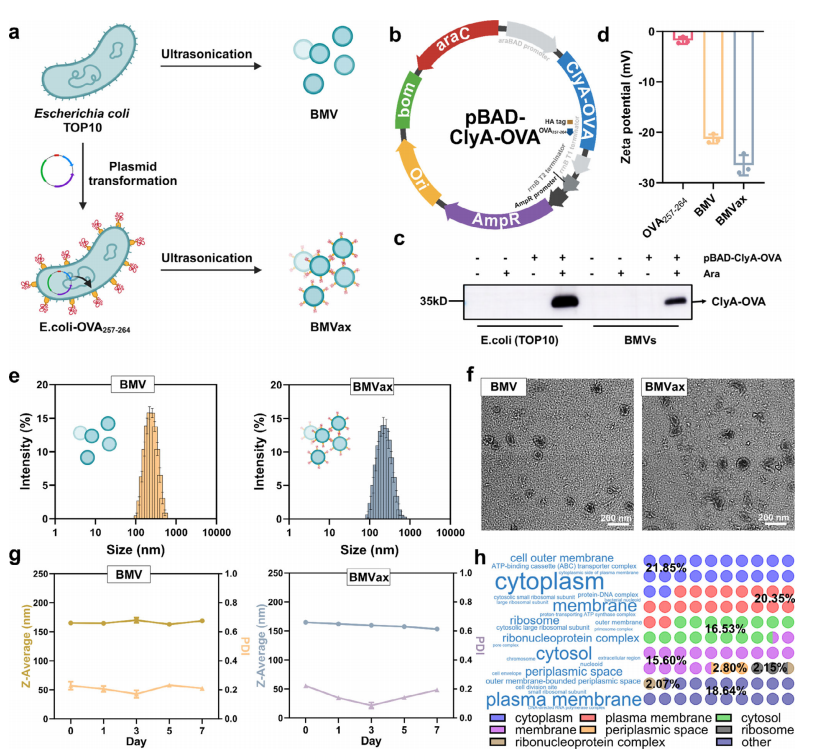
BMVax���Ʊ��������a) BMV��BMVax�Ʊ�����ʾ��ͼ��b) pBAD-ClyA-OVA�������Ŵ��ṹ��c) ���ÿ�HA�����ClyA-OVA�ںϵ��ױ�����е�Western blot������d) OVA257-264��BMV��BMVax��PBS�е�Zeta��λ��e) BMV��BMVax��PBS�е������ֲ���f) BMV��BMVax����羵ͼ��g) ��ͬʱ���BMV��BMVax��PBS�е�Zƽ����������ɢָ����PDI����h) ͨ��LC-MS/MS������BMVax�в�ͬ���������������������Ծ�ֵ�������ʾ��n=3��
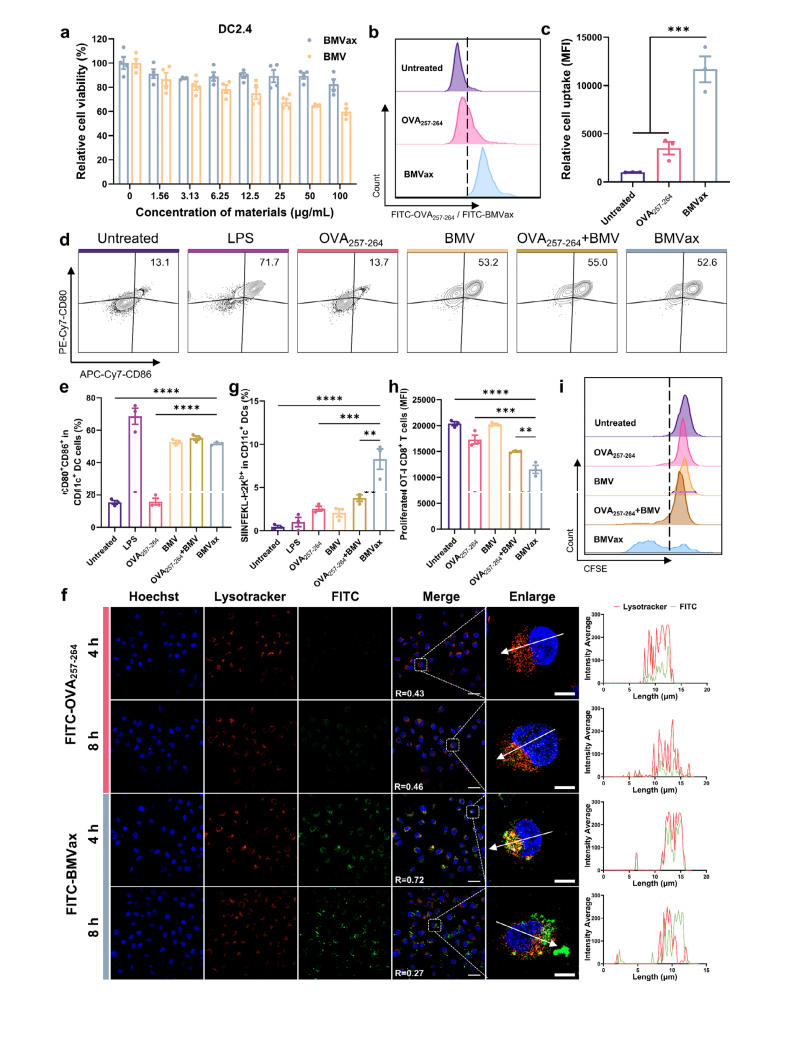
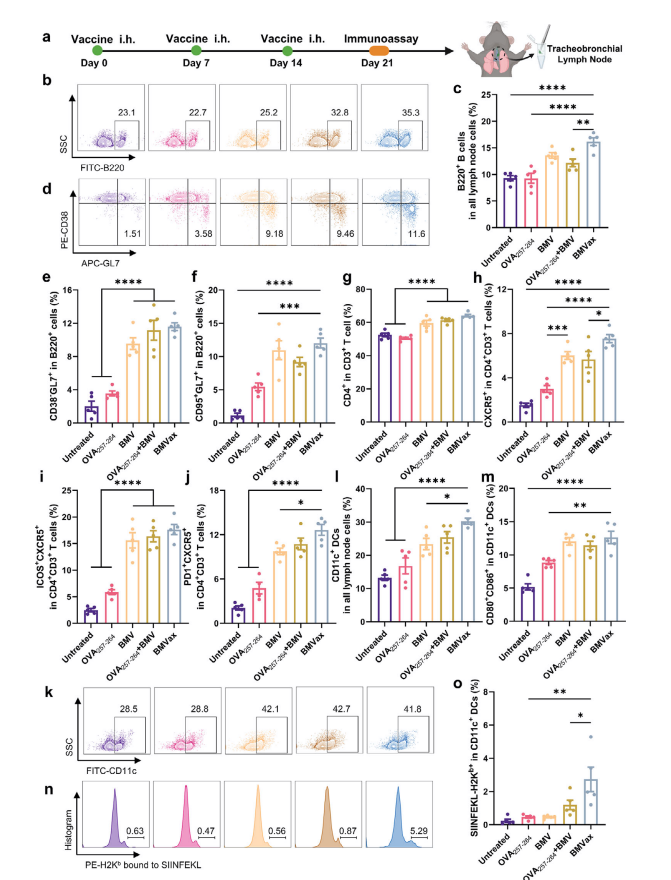
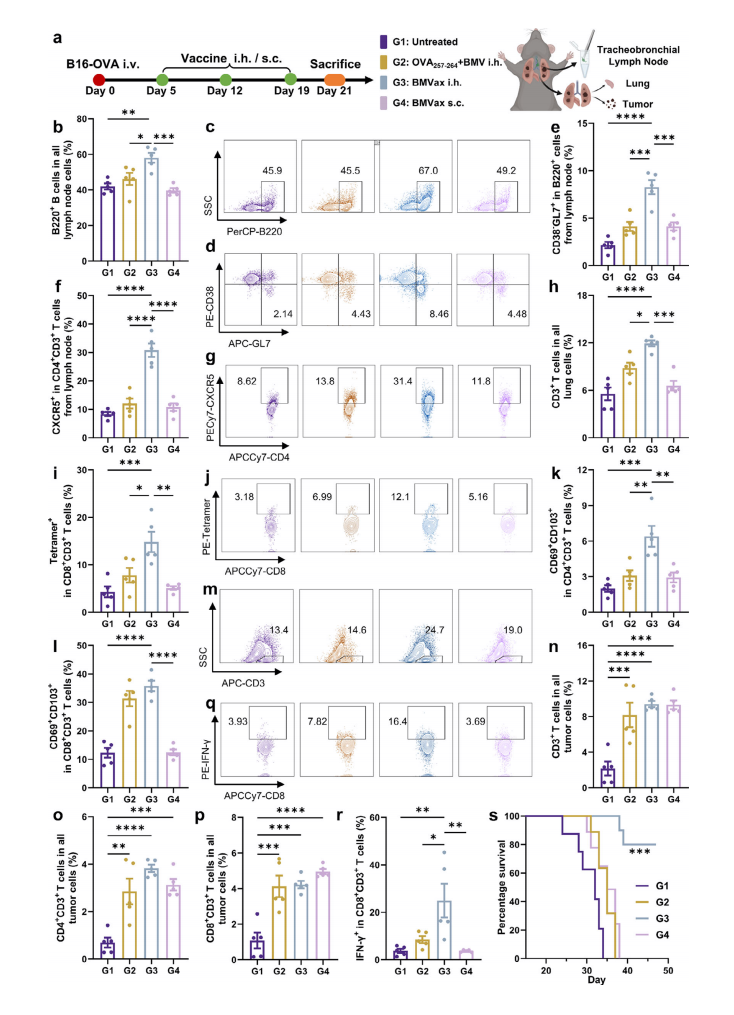
������BMVax���������յ�������֧�����ܰͽ��������߷�Ӧ������a) ����BMVax�������紥�����������߷�Ӧ��ʵ��ʱ���ߡ�b��c) ��������ʽϸ��ͼ(b)��ʾ��ͬ������С���ܰͽᵥϸ����Һ��B220+ Bϸ���ı�����ͳ��ѧ����(c)��ʾ�ܰͽ���ϸ��Ⱥ��B220+ Bϸ���ı�����d��e) ��������ʽϸ��ͼ(d)��ͳ��ѧ����(e)��ʾB220+ϸ����CD38−GL7+ϸ���ı�����f) ͳ��ѧ������ʾB220+ϸ����CD95+GL7+ϸ���ı�����g) ͳ��ѧ������ʾCD4+ϸ����CD3+ Tϸ���еı�����h) ͳ��ѧ������ʾCD4+CD3+ Tϸ����CXCR5+ϸ���ı�����i��j) ͳ��ѧ������ʾCD4+CD3+ Tϸ���� ICOS +CXCR5+ϸ��(i)��PD1+CXCR5+ϸ��(j)�ı�����k�Cm) ��������ʽϸ��ͼ(k)��ʾ��ͬ������С���ܰͽᵥϸ����Һ��CD11c+ DCs�ı�����ͳ��ѧ������ʾCD11c+ DCs���ܰͽ���ϸ��Ⱥ(l)��DCs��CD80+CD86+ϸ��(m)�еı�����n��o) ��������ʽϸ��ͼ(n)��ͳ��ѧ����(o)��ʾCD11c+ DCs��siinfekl-H2Kb+ϸ���ı����������Ծ�ֵ�������ʾ(n = 5)��ͳ��ѧ������ͨ��GraphPad Prism�����еĵ����ط��������one-way ANOVA�����㡣
�ܽ�
���Ƕ��ְ�֢ת�Ƶ���Ҫ��λ������ͳƤ�����������ڷβ��շ��ֲ�����Ӧ��Ϊ�����һ���⣬�о���Ա������һ�ֻ��ڹ���ϸ��Ĥ���ݵĿ������������硪��BMVax����ͨ�����̸���Ĵ˾�����ClyA-OVA��ԭ���γɾ��о������׳ߴ�������ȶ��Ե�Ĥ���ݣ�����Ч�������ߴ̼������뿹ԭ��
�ڶ���ʵ���У�����BMVax��������������֧�����ܰͽ��е�����ϸ����������������Bϸ�������ݸ���Tϸ���ͳ�����ͻ״ϸ�������ڷ���֯�д�����ӿ�ԭ������Tϸ���������ں�ɫ������ת��ģ���У�BMVax���ֳ������Ԥ��������Ч����ʵ��83.3%����ȫԤ���ʣ���������Ƥ�½��֡������粻�����յ��ֲ�ǿЧ����Ӧ�𣬻��ܴٽ�ϵͳ�������䣬Ϊ������Է�ת�ƵĿ����방֢�����ṩ���²��ԡ�
�ο����ף�
DOI: 10.1002/adma.202506174
 |
 |
 |
 |
| ��ά����Frontier | �������ײ���ǰ�� | MXenes Frontier | ����ҽѧFrontier |

| ��ܰ��ʾ�����������²ĿƼ�����Ӧ��Ʒ�����ڿ��У������������塣������վʾ��ͼԴ�Ի�������ͼƬ�����ο�������ʵ�ʲ��Խ��Ϊ��������Ȩ����ϵ��������ɾ������Ʒ���������ο�������ʵ��ֵΪ�� |
|
��Ȩ���� © 2019 ���������²ĿƼ�����˾
All rights reserved. ��ICP��16054715��-2 |
ɨһɨ