��֢�о����ٷ�չ�������е����·�չʹ���������ɶ�δ������ϣ�����Ȿ����Science�ڿ���������Ա��־���о����ļ������ؽ����������������Ʒ�����ǿҩ����ͣ�ȷ���µ����ưб꣬�˽����������Լ����ƻ��߷�Ӧ����Ľ�չ�� �����۱༭���Ը��ؿ���ȫ��10ƪ���Ľ��м�Ҫ������Թ����ѧϰ�ͽ�����
1. Science����������CAR-Tϸ������ʵ��������ƿ��

Ƕ�Ͽ�ԭ���壨CAR��-Tϸ�������Ʒ�������ijЩѪҺ������dz��ɹ���Ȼ�������ַ�������ʵ����һֱ����ս����������Ϊ���Խ����ܸ����Tϸ������������λ����ʡ����ѧԺDarrell J. Irvine���������һ��������ԣ�ͨ��ֱ������Ȼ�ܰͽ����������´̼�CAR�����CAR-Tϸ���Ĺ�Ч��
ע��ġ�amph-���塱����ɴٽ��ϳɿ�ԭ�ijʵݣ�������CAR-Tϸ��������������ӵ�����ɱ��������ϵͳ���ܻ�Ӧ������ǿ�κ�CAR-Tϸ���� 
Ma L, et al. Enhanced CAR�CT cell activity against solidtumors by vaccine boosting through the chimeric receptor. Science.2019;365(6449):162-8.DOI:10.1126/science.aav8692https://science.sciencemag.org/content/365/6449/162
2. Science����֢ͨ��DNAͻ�����ӱܰ�������

����ϸ����Ⱦ��ҽ�������ư�֢��ҽ��ͨ������һ����ͬ����ս����ҩ�Եķ�չ��������֪����ϸ����¶�ڿ�����ʱ�����ǻ���ʱ������ͻ���ʣ�����Ӧ�����ԣ����Ӷ������˺�������ؿ���ϸ�����ֵĻ��ᡣ��ô����ϸ���Ƿ�Ҳ�������ƵĻ�����ȷ��������ҩ�ﱩ¶�����������أ� ��Ϊ�ձ�Ĺ۵���Ϊ��������ҩ���Ǽȳ���ʵ���������ƿ�ʼʱ����֢�Ѿ�������ҩͻ��ϸ���� �м��ڴˣ���������ϰ��尩֢�о���Alberto Bardelli��Mariangela Russo�����о��������ֱ������CRC��ϸ���Ƿ�ͬ����������ϸ������Ӧ���ױ������ӱ�����ѹ�������Ƿ��ֱ�Ƥ�����������壨EGFR��/BRAF���Ƽ��µ��˴�������MMR����ͬԴ����DNA������ͬʱ�ϵ�����ҩ��persister��ϸ�����׳����ľۺ�ø�������ƹ����У�MMR�����ڻ�����Դ��������ֲ��������걾��Ҳ���µ��ˡ�EGFR/BRAF���Ƽ�����DNA���ˣ��ױ�����ǿ�����������Dz��ȶ��ԡ���ˣ���ϸ��һ������ϸ��Ҳ����ͨ����ǿ��ɱ�������Ӧ����ѹ���� 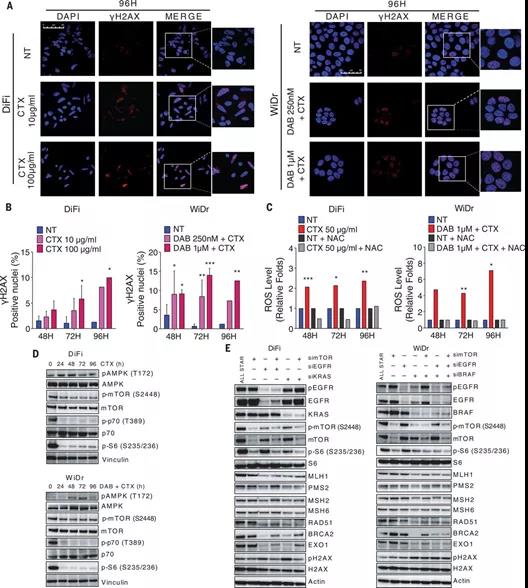
RussoM, Crisafulli G, Sogari A, Reilly NM, Arena S, Lamba S, et al. Adaptivemutability of colorectal cancers in response to targeted therapies. Science.2019;366(6472):1473-80.DOI:10.1126/science.aav4474https://doi.org/10.1126/science.aav4474
3. Science Advances����Ч����ѡ����������������������˫��������

���������Ʒ��ڶԿ���֢������й�����ǰ������������������������������ȫ���������µ�������Ч���谭�˰�֢�����Ʒ��Ĺ㷺Ӧ�á��ڴˣ�̨������廪��ѧ�퍾���̨����������о�ԺShu-Yi Lin����������һ����������Ʒ������Ʒ�ʹ�ø�Ч�Ҿ�������ѡ���ԵĻ�����������߿�����Ч�����ȫ�����ԡ� �������о��У�����˾���������ह��ܻ���״����ӵ���������֬����״���������ƣ�TT-LDCP����������NPs������������ͨ����������ػ���Ĵ̼����ӣ�STING��cGAS;����������ʾ����ǿ�Ļ������������һ����������������ԡ�TT-LDCP NPs���ϸ������HCC�������������������PD-L1�����ߴ̼���IL-2��������DNA��siRNA�����������������CD8+ Tϸ���Ļ����ǿ�˰�֢���������Ʒ���Ч������������HCC�������ù��������������ʵ�ֵ�siRNA������DNA˫�ص��ͣ���ѡ��������ر�������������������Ը��ư�֢�������ơ� 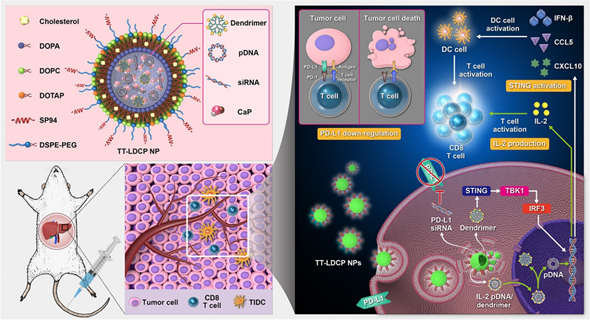
HuangK-W, et al. Highly efficient and tumor-selective nanoparticles fordual-targeted immunogene therapy against cancer. Science Advances.2020;6(3):eaax5032.DOI:10.1126/sciadv.aax5032https://advances.sciencemag.org/content/6/3/eaax5032
4. Science Advances����ϸ�������ݱ��ͱ仯���Լ���ɫ�������������

ʵʱ������֢���ߵİ������ƿ����ṩ�й���ҩ�Է�չ�������ƽ������Ҫ��Ϣ��ϸ�������ݣ�EVs������ѳ�Ϊ��ϣ���İ�֢�����־�����EV������ʾ��������Ʒ�Ӧ�ľ�DZ�����ڴˣ��Ĵ�������ʿ����ѧMatt Trau�������ѧYuling Wang����չʾ��ʹ�ö���EV���ͷ�����оƬ��EPAC��������Ѫ��EV�����ݱ�Ļ������Ʒ�Ӧ�Ŀ����ԡ� EPAC������������ǿоƬ�Ͷ��ر�����ǿ����ɢ�䣨SERS�����ױ�ǩϵͳ������ֱ��EV���ͷ���������EV���������ٴ�ǰģ���У��о���Ա�۲쵽EV���������ԺͶ����ƵIJ�ͬ���ͷ�Ӧ�����⣬�о���Ա�ɹ��شӺ���������Ѫ���м����˰�֢�����Ե�EV���͡��������˰������ܰ������Ƶĺ�ɫ�������ߵ�EV�����ݱ䣬������������ҩ�Է�չ�йص��ض�EV�ף���ӳ��EV���ͼ�����Ʒ�Ӧ��DZ���� 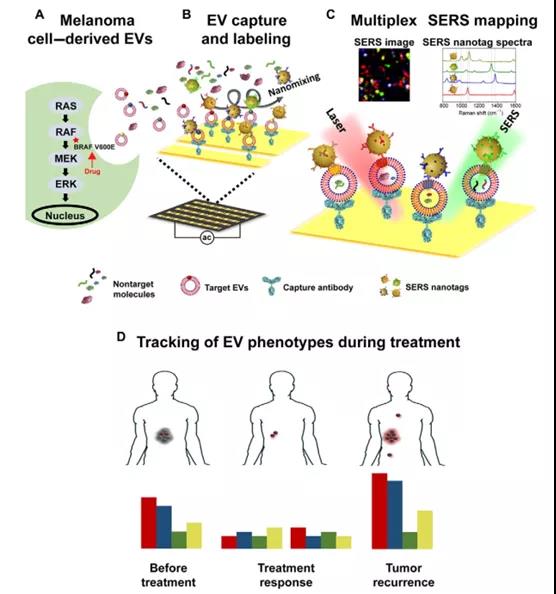
WangJ, et al. Tracking extracellular vesicle phenotypic changes enables treatmentmonitoring in melanoma. Science Advances. 2020;6(9):eaax3223.DOI:10.1126/sciadv.aax3223https://advances.sciencemag.org/content/6/9/eaax3223
5. Science Immunology������ϸ����PD-1�İ���ȱʧ���յ�����������


��Կ�����תTϸ���Ľߵij�����ϸ����������1��PD-1���������Ʒ��Ѿ����ı��˰�֢�����ơ�PD-1��Tϸ���������壬�ǰ�֢�����Ʒ��İб꣬Ҳ��������ϸ���ϱ��Ŀǰ�в����������������Tϸ��������PD-1�����ڿ����������е����ã���Ϊ������о���ʹ����PD-1��Ͽ����������PD-1 KOС�� �ڴˣ�ͨ������Pdcd1 floxedС����������ɾ��Tϸ�������ϸ���е�PD-1�������ѧҽѧԺVassiliki A. Boussiotis������������ǰû�б���ʶ����PD-1������ϸ���ϱ�������ƿ��������ߵ����á����Ƿ���������ϸ����ѡ�����г�PD-1������PD-1��ȱʧһ����Ч�������������������������Ѿ�֤��PD-1�ڵ�������ϸ���ķ��������е���Ҫ�ԡ����ܸ��о���δ����PD-1��Tϸ���Ľ��е����ã����о����Ҫ����������˼����PD-1Ϊ���ĵ��Ʒ���η������á� 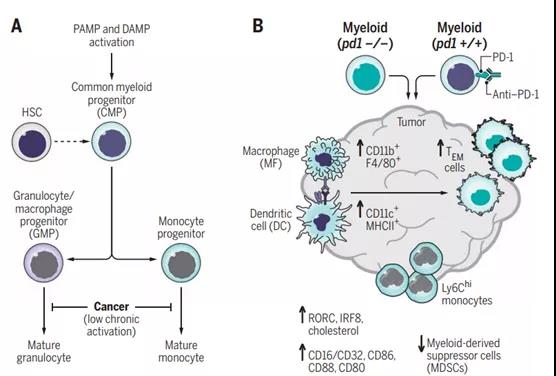
Strauss L, et al. Targeted deletion of PD-1 in myeloid cellsinduces antitumor immunity. Science Immunology. 2020;5(43):eaay1863.DOI:10.1126/sciimmunol.aay1863https://immunology.sciencemag.org/content/5/43/eaay1863
6. Science Immunology����ʾCAR-T�Ʒ�������֢���ӷ籩�Ļ���

ϸ�������ͷ��ۺ�����CRS�����방֢���ߵ�Ƕ�Ͽ�ԭ���壨CAR��Tϸ���Ʒ���صIJ���֢������CRS�Ļ����в���������й�ҽѧ��ѧԺ����ҽѧ�о����Ʋ����ڵ���������������ϸ�����������У��ɿ���Gasdermin E��GSDME�������ã���������CRS�� CARTϸ���ͷų�����øB������øB��������춬ø3���и������ϸ���е�GSDME������ϸ��������GSDME�����ϸ���������¾���ϸ����caspase 1��GSDMD�ļ������ڴ���CRS������Ҫ����֢������GSDMEˮƽ������CRS���س̶ȳ�����ء����⣬CAR Tϸ���յ�ϸ���������������ͷŵĴ����غͿ���øB��ˮƽ�йء� 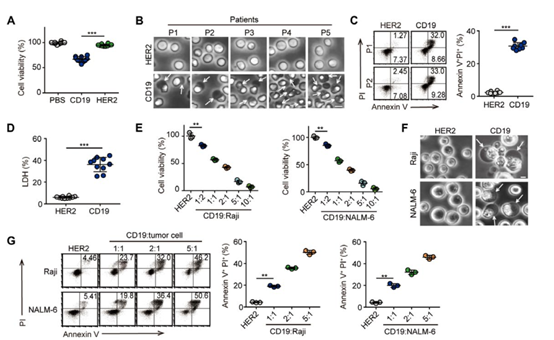
LiuY, et al. Gasdermin E�Cmediated target cell pyroptosis by CAR T cells triggerscytokine release syndrome. Science Immunology. 2020;5(43):eaax7969.DOI:10.1126/sciimmunol.aax7969https://immunology.sciencemag.org/content/5/43/eaax7969
7. Science Signaling����������Ƶ�KRASͻ�����λ���������Է�Ӧ��ϵͳ����

����KRAS G13Dͻ����Ľ�ֱ������CRC������ͨ����������������EGFR������з�Ӧ����������������KRASͻ�����CRC������û�С���Ϊ����֪��EGFR-RAS����ѧ�������������������õ�ԭ���в�����������ٴ�ʵ��ͨ���ܾ�������������KRASͻ��CRC���ߡ� ���ǣ����������������о���Edward C. Stites����ʹ���ۺϼ�������ﻯѧ������ʾ��������KRASͻ�䵰����ȣ�KRAS G13D�뵰��NF1�������̫�������ܾ����Ե�����������ˣ�KRAS G13Dϸ���е�Ұ����RAS��Ȼ������EGFR�Ļ������������������Щ���ֽ�ʾ��Ϊʲô��ҽѧ���Ӹ����ϵͳ��������ǻ����鼶��Ļ������档 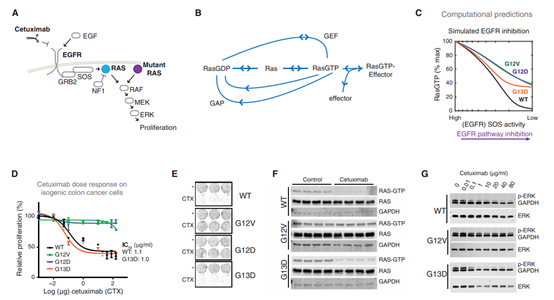
McFallT, et al. A systems mechanism for KRAS mutant allele�Cspecific responses totargeted therapy. Science Signaling. 2019;12(600):eaaw8288.DOI:10.1126/scisignal.aaw8288https://stke.sciencemag.org/content/12/600/eaaw8288
8. Science Signaling��֬��ϸ���ɴ�������ת��

�ں�ɫ�������ߵ������У������ƺ���Ƥ���ϱ�Ƥ�����������������������ǵ���������������֬����֬�����Ľ����ʱ����ת��Ϊ��ֱ�Ľ����ڡ���ɫ������ά���ѧCarmit Levy�����о��˺�����ϸ����֬��ϸ���Ĺ���������ȷ����֬��ϸ��������ת��ת���е�ֱ�����á� ���߷��֣�֬��ϸ������ϸ�����ӣ�ͨ��������ϸ���ϵ����巢���źţ��Ӷ���������Щ�ٽ���ֳ��������Ϯ�Ա��͵�microRNA�ı��microRNA��������������TGF-�µ���������������ת���Լ����йأ�������Ƥ��ḻ�����TGF-���źŴ�����ֹ�������ĺ�ɫ����ϸ������Ϯ��ת������˿������ƻ��ߵ�ת�ơ� 
Golan T, et al. Adipocytes sensitize melanoma cells toenvironmental TGF-�� cues by repressing the expression of miR-211. ScienceSignaling. 2019;12(591):eaav6847.DOI:10.1126/scisignal.aav6847https://stke.sciencemag.org/content/12/591/eaav6847
9. Science Translational Medicine������ҩ����ܲ�����������Ϊ������������

97%�������ٴ������в��Ե�ҩ����Ӧ֢��Դ�δ�������ʳƷ��ҩ������ֵ�������Ȼȱ����Ч�ͼ��������Զ���������ʧ�ܵ����ԭ��Ϊ����ô����ҩ��������Щ�����ԭ���в������ ����CRISPR-Cas9ͻ�似����������Ȫ��ʵ����ason M. Sheltzer�������ٴ�����IJ�ͬ�Σ��о���һϵ�п���ҩ���ҩ��е㡣ȷ���˵��¸������һ��DZ��ԭ�����ٴ������е�ijЩ������ʵ���ϲ�δ���������Ϊ���ǰ�����°����� Ȼ���о���Աȷ���˶��ִ������������ҩ����ҵ�������һ��ҩ�����ȷ�б꣬������ڽ��������ٴ�֮ǰ����Ҫ������о����ϸ�ķ�������֤DZ��ҩ��İбꡣ 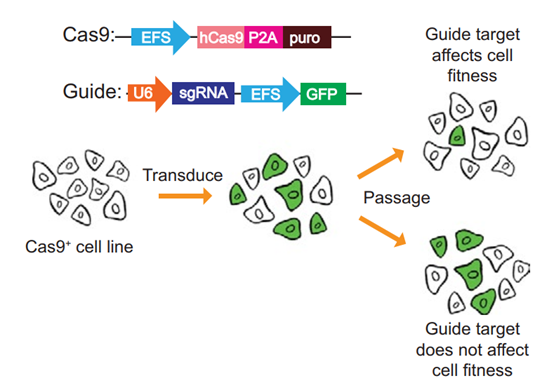
Lin A, et al. Off-target toxicity is a common mechanism of action ofcancer drugs undergoing clinical trials. Science Translational Medicine.2019;11(509):eaaw8412.DOI: 10.1126/scitranslmed.aaw8412https://stm.sciencemag.org/content/11/509/eaaw8412
10. ScienceTranslational Medicine����������������V��1+ �æ� Tϸ���������ڻ������������ٰ�

��֪�ض��Ħæ� Tϸ����Ⱥ���������Ƥ���ͳ�������֯��Ϊ��ȷ���æ� Tϸ���������ٰ���⣬Ӣ���ع���ѧԺAdrian Hayday��������������֯�������������з����ϸ���������ڽ���������������֯��������֯�й۲쵽����ϸ����������V��1+ Tϸ������һСȺ���������ٰ���Ů�ķ�����������ЩV��1+ Tϸ���벡�黺�������������ء���Щ���������������֯פ���Ħæ� Tϸ������Ӱ�����ٰ��Ľ�չ����Щϸ�����������л�δ�������Ʒ���Ԥ�Ĺؼ��� 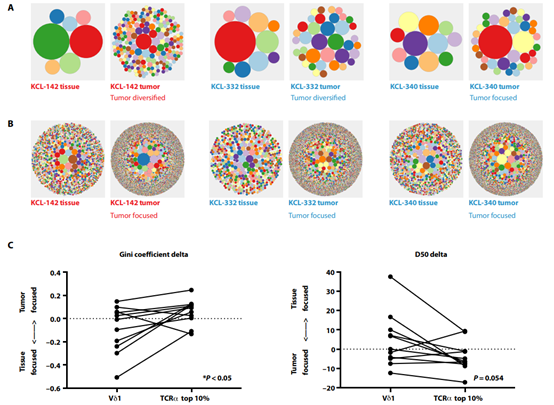
Wu Y, et al. An innate-like V��1+ �æ� T cell compartment in thehuman breast is associated with remission in triple-negative breast cancer. ScienceTranslational Medicine. 2019;11(513):eaax9364.DOI: 10.1126/scitranslmed.aax9364https://stm.sciencemag.org/content/11/513/eaax9364 
�ο����Ϻ����ص�ַ��http://promo.aaas.org/images/Publishing/Journals/2020/Booklet/AACR20_Cancer_Booklet_Online-Final.pdf
��Ϣ��Դ��������
����ϢԴ�Ի���������ѧ������ ������Ȩ����ϵ��������ɾ��
























 ѧ��ǰ��
ѧ��ǰ��
